O modelo prescritivo baseado em “doses padrão” e médias populacionais tornou-se obsoleto diante da Medicina Personalizada. Na terapêutica endocanabinoide, protocolos fixos de peso ou idade não são suficientes para definir a conduta. Este artigo explora como a farmacogenômica (polimorfismos do citocromo P450), a farmacodinâmica (curvas de resposta bifásica) e o Efeito Comitiva comprovam que a singularidade biológica do paciente exige titulação individualizada. Descubra por que abandonar a padronização e buscar a Dose Mínima Efetiva é o verdadeiro núcleo da prática clínica moderna.
A Transição para a Medicina 3.0: O Declínio Definitivo da “Dose Padrão”
A transição da medicina convencional para a chamada Medicina 3.0 — centrada em personalização, previsibilidade e precisão biológica — consolida o declínio definitivo da lógica da “dose padrão”. Durante décadas, o raciocínio prescritivo foi estruturado a partir de moléculas isoladas, com alvos farmacológicos específicos e faixas posológicas relativamente fixas, ajustadas de forma simplificada por peso corporal ou idade. Esse modelo mostrou-se funcional para fármacos de mecanismo único e farmacocinética previsível.
Entretanto, a incorporação terapêutica da Cannabis sativa e o aprofundamento científico do Sistema Endocanabinoide (SEC) evidenciaram as limitações desse paradigma. O SEC atua como sistema modulador central da homeostase, regulando dor, inflamação, humor, sono, apetite e resposta ao estresse.¹ Ao intervir nesse sistema, o médico não está bloqueando um receptor isolado, mas modulando uma rede neuroimunoendócrina dinâmica e individualizada.
Nesse contexto, a padronização rígida de dose torna-se conceitualmente frágil. No manejo de condições crônicas e refratárias, a “dose padrão” pode ser simplesmente a dose inadequada para a maioria dos pacientes.
O que é a medicina personalizada?
A Medicina Personalizada — também denominada medicina de precisão — é um modelo assistencial que substitui a lógica da padronização terapêutica pela adaptação individual das condutas clínicas. Seu princípio central é simples, porém transformador: indivíduos com o mesmo diagnóstico não são biologicamente iguais e, portanto, não devem necessariamente receber a mesma intervenção na mesma dose.
Tradicionalmente, a prática médica foi estruturada sobre médias populacionais derivadas de ensaios clínicos. Protocolos são construídos a partir da “resposta média” observada em grupos heterogêneos, e posteriormente aplicados de maneira relativamente uniforme. A medicina personalizada não rejeita essa base científica, mas reconhece sua limitação: a média estatística não representa o indivíduo real sentado no consultório.
Nesse modelo, decisões terapêuticas passam a considerar múltiplas camadas de informação biológica e clínica, incluindo:
- Variabilidade genética (farmacogenômica)
- Perfil metabólico e inflamatório
- Características fenotípicas
- Microbiota intestinal
- Estilo de vida e exposições ambientais
- Interações medicamentosas
A farmacogenômica constitui um dos pilares dessa abordagem, ao estudar como polimorfismos genéticos influenciam absorção, distribuição, metabolismo e resposta aos fármacos. Variações em enzimas metabolizadoras, transportadores ou receptores podem alterar significativamente a eficácia terapêutica e risco de eventos adversos.

Contudo, Medicina Personalizada não se restringe ao teste genético. Ela envolve integração clínica sofisticada: interpretar sinais, contexto, comorbidades e dinâmica fisiológica para construir uma estratégia terapêutica ajustada à biologia do paciente.
Do ponto de vista conceitual, trata-se de uma mudança de eixo:
- Da padronização → para a estratificação
- Da média populacional → para a assinatura biológica individual
- Do bloqueio sintomático → para a modulação fisiológica
Em áreas como oncologia, imunologia e neurologia, essa transição já é realidade consolidada. No campo da medicina endocanabinoide, ela deixa de ser inovação e passa a ser necessidade, dada a expressiva variabilidade interindividual na resposta aos fitocanabinoides.
Em termos práticos, a Medicina Personalizada só se concretiza quando o raciocínio biológico se traduz em decisão terapêutica individualizada. É no momento da prescrição que a teoria abandona o campo conceitual e passa a impactar diretamente o desfecho clínico.
E é justamente nesse ponto que o primeiro grande deslocamento ocorre.
Em termos práticos, a Medicina Personalizada deixa de ser apenas um constructo teórico quando o raciocínio biológico se transforma em decisão terapêutica concreta. Não basta reconhecer a variabilidade genética, metabólica ou inflamatória — é preciso incorporá-la ao ato prescritivo. É no momento da escolha da formulação, da definição da estratégia de titulação e do acompanhamento longitudinal que a teoria abandona o plano conceitual e passa a influenciar diretamente o desfecho clínico.
É exatamente nesse ponto que ocorre o primeiro grande deslocamento de paradigma: a transição da prescrição baseada em protocolos fixos para a prescrição orientada por fisiologia individual. Na medicina endocanabinoide, essa mudança torna-se ainda mais evidente, pois o alvo terapêutico não é um sintoma isolado, mas uma rede regulatória complexa e dinâmica.
Para compreender plenamente a arquitetura e a função dessa rede neuroimunoendócrina que a Medicina 3.0 busca modular — e não simplesmente bloquear — revise nosso post O que é o Sistema Endocanabinoide? – WeCann Academy. Essa base conceitual é fundamental para entender por que a dose padrão perde sustentação quando confrontada com a biologia real do paciente.
Nível Clínico: a busca pela Dose Mínima Efetiva
A primeira ruptura de paradigma não acontece no laboratório — acontece no consultório. É no encontro clínico que a lógica da dose fixa começa a perder sustentação.
Na terapêutica canabinoide, peso corporal e idade raramente constituem determinantes primários da posologia. Embora a cannabis apresente ampla janela terapêutica, a variabilidade interindividual é marcante e clinicamente relevante. Pacientes com o mesmo diagnóstico, perfil fenotípico semelhante e intensidade sintomática comparável podem demandar doses substancialmente diferentes para atingir desfechos equivalentes.¹
Essa heterogeneidade decorre do fato de que o alvo terapêutico não é apenas o sintoma isolado, mas a modulação do tônus endocanabinoide basal — variável conforme carga inflamatória, exposição ao estresse crônico, comorbidades metabólicas, uso concomitante de fármacos e particularidades neurobiológicas individuais.
Diante desse cenário, o padrão-ouro da prática clínica abandona a prescrição rígida e adota titulação progressiva — start low, go slow — estratégia que permite identificar a Dose Mínima Efetiva: a menor quantidade capaz de produzir benefício clínico consistente com mínima ocorrência de efeitos adversos.²
A condução dessa titulação requer domínio técnico não apenas da dosagem, mas do perfil de segurança de cada paciente, das possíveis interações medicamentosas e da vigilância ativa de efeitos adversos. Antes de prescrever a primeira gota, acesse nosso Guia rápido: Como orientar seu paciente sobre cannabis medicinal e estruture sua abordagem clínica com segurança e previsibilidade.
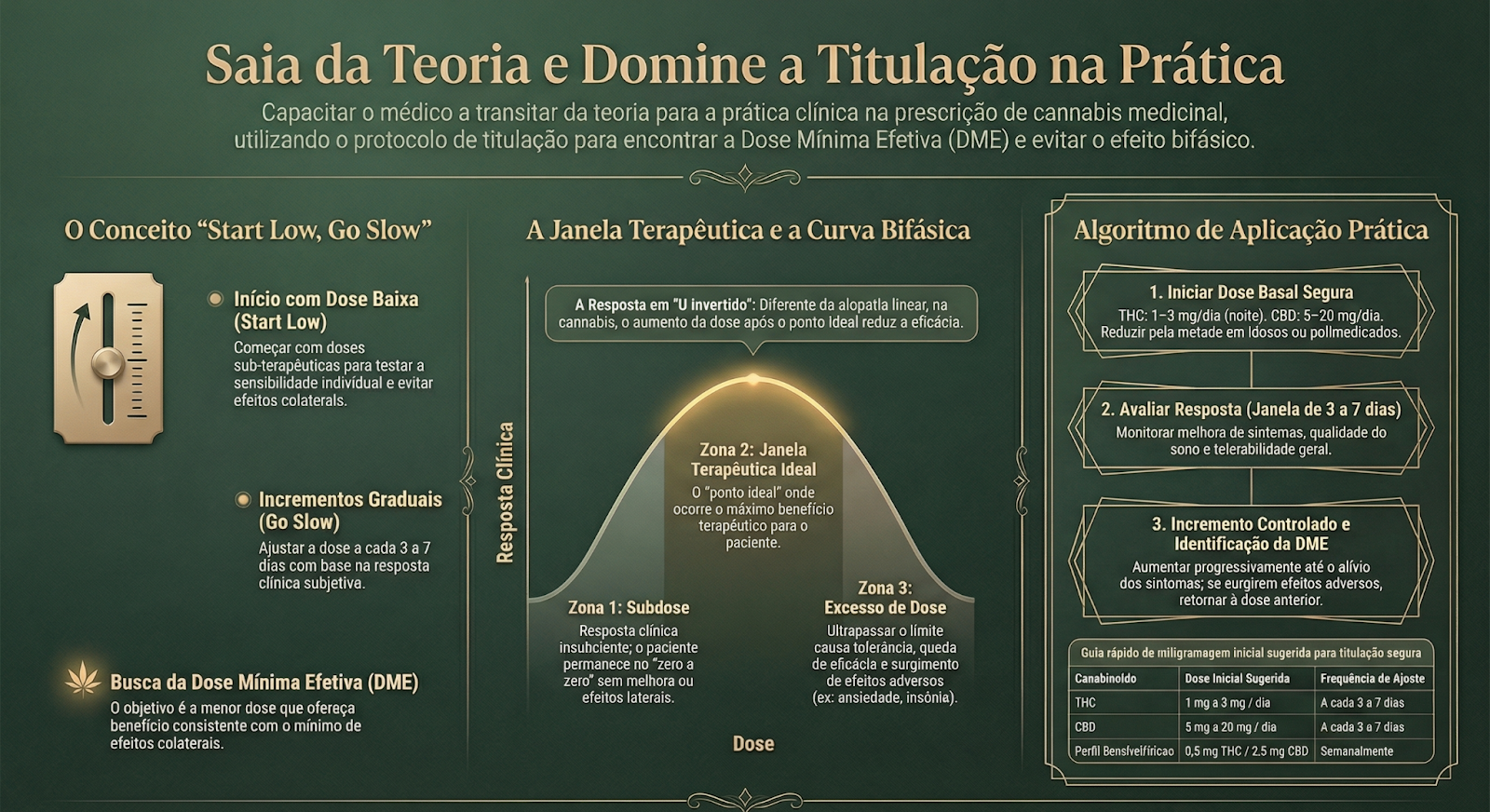
Nesse modelo, miligramas deixam de ser o centro da decisão. A resposta clínica funcional — melhora da dor, estabilidade do sono, redução de crises, ganho de qualidade de vida — passa a ser o verdadeiro parâmetro de ajuste. A dose não é o ponto de partida absoluto; é a consequência da escuta clínica qualificada e da leitura fisiológica individualizada.
Nível Farmacodinâmico: respostas bifásicas e efeito comitiva
A insuficiência da “dose padrão” torna-se ainda mais evidente quando aprofundamos a análise farmacodinâmica dos fitocanabinoides.
Diferentemente de muitos fármacos clássicos, cuja relação dose–resposta tende a seguir um padrão linear ou log-linear, canabinoides como THC e CBD frequentemente apresentam curva bifásica, descrita como um “U invertido”.³ Isso significa que o efeito terapêutico não aumenta indefinidamente com a elevação da dose.
Em faixas baixas a intermediárias, observam-se benefícios como analgesia, relaxamento, melhora do sono e modulação ansiolítica. No entanto, ao ultrapassar o intervalo terapêutico individual, a eficácia pode declinar e efeitos paradoxais podem surgir— incluindo ansiedade, insônia e irritabilidade.
Nesse contexto, a máxima de que “mais é melhor” deixa de ser imprecisa e passa a ser potencialmente iatrogênica. A dose excessiva não apenas perde eficiência; pode comprometer o resultado clínico global e reduzir a adesão terapêutica.
Outro elemento determinante é o perfil fitoquímico da formulação. O chamado Efeito Comitiva (entourage effect) descreve a interação sinérgica entre canabinoides, terpenos e flavonoides.4 Essa sinergia pode modular afinidade receptorial, biodisponibilidade e perfil de efeitos adversos.
Dados oriundos de metanálise observacional envolvendo 670 pacientes com epilepsia refratária oferecem um argumento particularmente relevante para a discussão farmacodinâmica.5 Nessa análise, que incluiu 11 estudos clínicos com tempo médio de seguimento de 6,2 meses e doses variando entre 1 e 50 mg/kg/dia, aproximadamente 64% dos pacientes relataram melhora na frequência das crises (399/622).
Quando estratificados por tipo de formulação, observou-se maior proporção de melhora relatada entre pacientes tratados com extratos ricos em CBD (71%; 318/447) em comparação ao CBD purificado (46%; 81/175), com diferença estatisticamente significativa (p < 0,0001).5
O dado mais expressivo, entretanto, reside na dose média utilizada: pacientes em uso de extratos ricos em CBD receberam aproximadamente 6,0 mg/kg/dia, enquanto aqueles tratados com CBD isolado utilizaram, em média, 25,3 mg/kg/dia — uma diferença substancial. Paralelamente, eventos adversos leves e graves foram significativamente mais frequentes nos produtos contendo CBD purificado.5
Esses achados sugerem que extratos de espectro completo podem atingir eficácia clínica com doses consideravelmente menores e possivelmente com melhor tolerabilidade quando comparados ao composto isolado.5 Embora mais estudos ainda sejam necessários para confirmação definitiva, a hipótese mais plausível reside na interação sinérgica entre canabinoides e outros fitocompostos — o chamado efeito entourage.
Assim, a personalização farmacodinâmica não se limita ao ajuste quantitativo da dose. Ela exige decisão estratégica quanto à proporção THC:CBD, à presença de canabinoides minoritários, ao perfil terpênico e à escolha do quimiotipo mais coerente com o fenótipo clínico e o contexto fisiopatológico do paciente.
Nível de Precisão: farmacogenômica e variabilidade metabólica
No nível mais avançado da Medicina Personalizada, a “dose padrão” torna-se biologicamente insustentável.
O metabolismo dos canabinoides ocorre predominantemente por enzimas do citocromo P450 — especialmente CYP2C9, CYP2C19 e CYP3A4 — cuja expressão e atividade variam amplamente na população em função de polimorfismos genéticos.¹ Essa variabilidade impacta diretamente concentrações plasmáticas, meia-vida e risco de eventos adversos, mesmo quando a dose administrada é idêntica.
No contexto específico do canabidiol, evidências recentes reforçam a relevância clínica da farmacogenômica. Um estudo envolvendo 113 pacientes com epilepsia farmacorresistente avaliou a influência de variantes genéticas em farmacogenes relacionados ao metabolismo e transporte de fármacos sobre a resposta terapêutica ao CBD.6 Utilizando tecnologia de genotipagem em larga escala (Affymetrix Plus Array), os pesquisadores mapearam polimorfismos em enzimas metabolizadoras e transportadores de drogas.
Os resultados demonstraram que determinadas variantes genéticas estavam associadas a maior redução da frequência de crises epilépticas, sugerindo perfil de melhor resposta ao CBD. Em contrapartida, outros polimorfismos correlacionaram-se com maior incidência de eventos adversos, como sedação excessiva e alterações comportamentais.6
Esses achados sustentam uma premissa fundamental: a variabilidade clínica não é aleatória — ela possui base molecular identificável.
Além do metabolismo, variações em genes como CNR1, AKT1 e COMT também modulam sensibilidade aos canabinoides e vulnerabilidade a efeitos neuropsiquiátricos. Assim, o que para um paciente representa estabilidade clínica, para outro pode significar intolerância ou risco aumentado de efeitos adversos.
O Fim da Dose Padrão: quando a biologia individual redefine a terapêutica endocanabinoide
A chamada “morte da dose padrão” não representa a negação da ciência, mas sua evolução natural. À medida que o conhecimento sobre o Sistema Endocanabinoide, a farmacodinâmica dos fitocanabinoides e a variabilidade farmacogenômica se consolida, torna-se cada vez mais evidente que a padronização rígida é incompatível com a complexidade biológica humana. A média populacional, embora útil como ponto de partida metodológico, revela-se insuficiente como ponto de chegada clínico.
Na prática endocanabinoide, a dose deixa de ser um número previamente definido e passa a ser uma variável dinâmica, construída a partir da interação entre fenótipo clínico, tônus endocanabinoide basal, perfil inflamatório, contexto psicobiológico e arquitetura genética individual. A titulação progressiva, a escolha criteriosa do espectro fitoquímico e a consideração de polimorfismos metabólicos não são refinamentos opcionais — constituem o próprio núcleo da precisão terapêutica.
Os dados farmacodinâmicos que demonstram curvas bifásicas, o impacto do efeito entourage na redução de dose e na tolerabilidade, bem como as evidências farmacogenômicas associando variantes genéticas à resposta e aos eventos adversos do CBD, convergem para uma mesma conclusão: a variabilidade interindividual não é uma achado estatístico, é um determinante clínico.
Assim, a Medicina Personalizada na prática endocanabinoide não se limita a ajustar miligramas. Ela redefine o próprio conceito de prescrição. O foco desloca-se da intervenção padronizada para a modulação fisiológica individualizada; do protocolo fixo para a estratégia adaptativa; da dose média para a Dose Mínima Efetiva biologicamente coerente.
Pratique a Medicina do Século XXI
Se a medicina do século XX foi construída sobre a lógica da uniformidade, a medicina do século XXI consolida-se sobre a singularidade biológica. No contexto da medicina endocanabinoide, essa transição não é tendência futura — é exigência presente.
O profissional que permanece dependente de “receitas de bolo” e protocolos rígidos inevitavelmente encontrará limites clínicos diante da complexidade da Medicina Personalizada. A prática baseada apenas em médias populacionais já não responde aos desafios de condições crônicas, refratárias e biologicamente heterogêneas.
A Certificação Internacional em Medicina Endocanabinoide da WeCann Academy é o ambiente formativo onde o médico aprende a pensar de forma complexa, integrando farmacodinâmica, farmacogenômica e fisiologia do Sistema Endocanabinoide, mas atuar de maneira prática, estruturada e segura.
Domine:
- A farmacodinâmica e farmacogenômica aplicada aos canabinoides
- As interações medicamentosas clinicamente relevantes
- As estratégias de titulação nas mais diversas especialidades
- A identificação da Dose Mínima Efetiva em diferentes contextos clínicos
PRATIQUE UMA MEDICINA DE PRECISÃO: CONHEÇA A CERTIFICAÇÃO WECANN
Referências
- Montagner P, de Salas-Quiroga A. Tratado de Medicina Endocanabinoide. 1ª ed. WeCann Endocannabinoid Global Academy; 2023.
- MacCallum CA, Russo EB. Practical considerations in medical cannabis administration and dosing. Eur J Intern Med. 2018;49:12–19. doi:10.1016/j.ejim.2018.01.004.
- Graczyk M, Łukowicz M, Dzierzanowski T. Prospects for the Use of Cannabinoids in Psychiatric Disorders. Front Psychiatry. 2021 Mar 12;12:620073. doi: 10.3389/fpsyt.2021.620073. PMID: 33776815; PMCID: PMC7994770.
- Russo EB. Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. Br J Pharmacol. 2011;163(7):1344–1364. doi:10.1111/j.1476-5381.2011.01238.x.
- Pamplona FA, da Silva LR, Coan AC. Potential clinical benefits of CBD-rich cannabis extracts over purified CBD in treatment-resistant epilepsy: observational data meta-analysis. Front Neurol. 2018;9:759. doi:10.3389/fneur.2018.00759.
- Davis B.H., Beasley T.M., Amaral M., Szaflarski J.P., Gaston T., Perry Grayson L., Standaert D.G., Bebin E.M., Limdi N.A., UAB CBD Study Group (includes all the investigators involved in the UAB EAP CBD program) Pharmacogenetic Predictors of Cannabidiol Response and Tolerability in Treatment-Resistant Epilepsy. Clin. Pharmacol. Ther. 2021;110:1368–1380.
