A Síndrome de Hiperêmese Canabinoide (SHC) é uma condição paradoxal associada ao uso crônico de cannabis rica em THC, caracterizada por náuseas cíclicas, vômitos incoercíveis e dor abdominal. Seu mecanismo envolve o efeito bifásico dos canabinoides, com dessensibilização dos receptores CB1, alterações dopaminérgicas e disfunção do receptor TRPV1. Evidências recentes indicam suscetibilidade genética, especialmente em genes relacionados ao metabolismo do THC e à regulação da emese, o que diferencia a SHC de outras síndromes de vômitos cíclicos.
Veja nessa postagem
Definição e epidemiologia
A Síndrome de Hiperêmese Canabinoide (SHC) representa um desafio diagnóstico relevante na prática clínica contemporânea, especialmente em serviços de emergência. O paradoxo da condição chama atenção: embora os fitocanabinoides — em especial o delta-9-tetraidrocanabinol (THC) — sejam amplamente reconhecidos por suas propriedades antieméticas em contextos oncológicos e paliativos, a SHC surge justamente em usuários crônicos, manifestando-se por episódios cíclicos de náuseas intensas, vômitos incoercíveis e dor abdominal.1,2
Para o médico, compreender essa síndrome vai além da curiosidade fisiopatológica. Trata-se de uma competência clínica essencial para o diagnóstico diferencial, para a segurança do paciente e para a correta distinção entre o uso terapêutico controlado e o uso crônico desregulado — este último, associado ao desenvolvimento da síndrome.
Descrita formalmente em 2004 por Allen et al., na Austrália — com relatos retrospectivos desde 1996 — a SHC está fortemente associada ao uso diário ou semanal de cannabis de alta potência, por períodos prolongados, geralmente de anos.1,3
Estudos epidemiológicos sugerem que a síndrome é rara ou praticamente inexistente no contexto do uso medicinal supervisionado, no qual doses são tituladas, monitoradas e frequentemente baixas e balanceadas com outros canabinoides. Em contraste, a SHC ocorre predominantemente em indivíduos que consomem grandes e frequentes quantidades de THC e em consumidores de canabinoides sintéticos (como K2 e Spice), substâncias que atuam como agonistas totais dos receptores CB1, intensificando a estimulação canabinoide central.1,4
Fisiopatologia: o paradoxo do efeito bifásico
A etiologia da SHC desafia a noção clássica de que a cannabis é intrinsecamente antiemética. A explicação reside no efeito bifásico dos canabinoides, fenômeno bem descrito na farmacologia do THC:
- Doses baixas a moderadas: o THC exerce efeito antiemético por meio da ativação de receptores CB1 no núcleo do trato solitário e na área postrema, regiões centrais envolvidas no controle do reflexo do vômito.3,5
- Doses altas e uso crônico: a estimulação sustentada leva à downregulation dos receptores CB1, à saturação de tecidos lipídicos e à inversão do efeito farmacológico, convertendo a ação antiemética em pró-emética.5,6
Adicionalmente, o THC reduz a motilidade gástrica. Em contexto de uso crônico, esse efeito pode contribuir para gastroparesia funcional, distensão gástrica e perpetuação dos episódios de êmese.5 Ou seja, o que inicialmente “funciona” para náusea passa, com o tempo, a ser parte do problema.
Para saber mais sobre os canabinoides, acesse: Principais Fitocanabinoides e seus efeitos no organismo
Genética: suscetibilidade individual e mecanismos moleculares
Um avanço decisivo na compreensão da SHC veio com o maior estudo genômico da síndrome até o momento, conduzido por Russo et al. (2022). A análise identificou variantes genéticas estatisticamente significativas que diferenciam pacientes com SHC de pessoas com uso exacerbado de cannabis que nunca desenvolveram a condição.¹
Esses achados enfraquecem teorias anteriores que atribuíam a síndrome à contaminação por pesticidas (como óleo de Neem ou azadiractina) e sustentam o conceito de uma doença genética rara desmascarada pela exposição crônica ao THC.
As principais vias envolvidas incluem:
- Metabolismo de canabinoides (Fase I): mutações no gene CYP2C9, responsável pela metabolização do THC. Metabolizadores lentos acumulam níveis elevados de THC e metabólitos ativos, favorecendo toxicidade.¹
- Sinalização dopaminérgica: variantes nos genes COMT e DRD2. A dopamina desempenha papel central na fisiologia da êmese, e alterações em sua degradação ou recepção correlacionam-se com náusea intensa e comportamentos compulsivos.¹
- Receptor TRPV1 (TRPV1): envolvido na percepção térmica e nociceptiva. Essas mutações ajudam a explicar a resposta idiossincrática ao calor e à capsaicina.¹
- Transporte de colesterol (ABCA1): sugerindo participação da homeostase lipídica na fisiopatologia da síndrome.¹
A identificação dessas variantes genéticas (como CYP2C9 e TRPV1) transforma a SHC de um ‘evento aleatório’ em uma condição de risco estratificável. Essa análise molecular, que separa a toxicologia da terapêutica, é explorada no Tratado de Medicina Endocanabinoide. Se você busca compreender com propriedade o perfil de toxicidade e potenciais efeitos adversos dos canabinoides, esta é a referência bibliográfica que falta na sua estante. Acesse o Tratado e aprofunde sua base científica.
Diferentemente da Síndrome dos Vômitos Cíclicos (SVC), a SHC não apresenta associação com polimorfismos no gene CNR1 (receptor CB1), o que reforça tratar-se de uma entidade fisiopatológica distinta.7
Quadro clínico e fases da síndrome
A apresentação clínica da SHC é relativamente estereotipada e classificada em três fases:3,5
Fase prodrômica – Pode se estender por meses ou anos. O paciente apresenta náuseas matinais, desconforto abdominal e medo de vomitar, mantendo, em geral, a ingestão alimentar. Um ponto crítico é que muitos aumentam o uso de cannabis tentando aliviar os sintomas — perpetuando o ciclo.
Fase hiperemética – Caracteriza-se por episódios agudos e intensos de vômitos cíclicos, dor abdominal difusa, desidratação importante e risco de distúrbios hidroeletrolíticos e insuficiência renal aguda.
Fase de recuperação – Ocorre após a cessação do uso. Há resolução progressiva dos sintomas, recuperação ponderal e retorno do bem-estar.
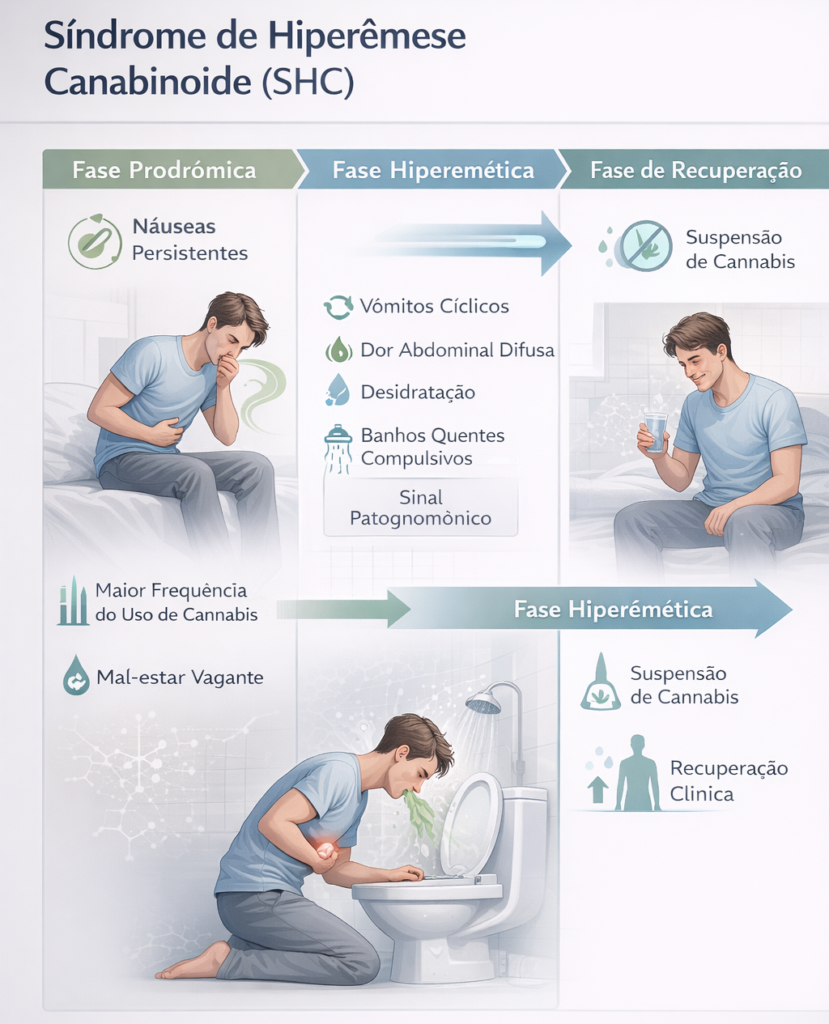
Sinal patognomônico: O comportamento de banhos quentes compulsivos (comportamentos de banho patológico) é um sinal patognomônico da SHC. Os pacientes relatam alívio significativo da náusea e da dor abdominal, provavelmente mediado pela ativação cutânea de receptores TRPV1, que modulam vias centrais da dor visceral e da êmese.1,8
Manejo terapêutico
O tratamento da SHC exige abordagem específica, uma vez que antieméticos convencionais, como antagonistas 5-HT3, frequentemente se mostram ineficazes.9
Fase aguda (emergência)
- Haloperidol intravenoso: demonstrou superioridade em relação à ondansetrona no controle de náusea e dor abdominal, reforçando o papel da via dopaminérgica na síndrome.9
- Capsaicina tópica: aplicada no abdômen, atua como agonista do TRPV1, mimetizando o efeito dos banhos quentes e contribuindo para a modulação da motilidade gástrica.8
- Suporte clínico: reposição volêmica agressiva e correção de distúrbios eletrolíticos.
Manejo de longo prazo
- Abstinência completa: é o único tratamento definitivo. A reexposição ao THC, mesmo em doses menores, leva quase invariavelmente à recorrência dos sintomas.3,5
- Educação do paciente: explicar a base genética da suscetibilidade é fundamental para desfazer a crença de que a cannabis está “tratando” a náusea, quando, na verdade, é o fator causal.1,2
Para saber como orientar seus pacientes a respeito do uso da cannabis medicinal, acesse: Guia rápido: Como orientar seu paciente sobre cannabis medicinal
Implicações para a prática médica
A Síndrome de Hiperêmese Canabinoide é uma condição clínica específica, associada predominantemente à exposição crônica, desregulada e alta de THC, em indivíduos geneticamente suscetíveis. Essa distinção não é semântica — ela é fundamental para a segurança do paciente e para a boa prática médica.
As evidências disponíveis indicam que a SHC é rara ou inexistente em contextos de uso medicinal supervisionado, nos quais há titulação de dose, acompanhamento clínico e escolha racional de formulações.
Conhecer a SHC é fundamental para evitar atrasos diagnósticos e decisões terapêuticas imprecisas, especialmente no ambiente de emergência. O comportamento de banhos quentes compulsivos, a refratariedade aos antieméticos convencionais e a história de uso crônico de produtos com alta concentração em THC são os elementos centrais para o diagnóstico. A reposição volêmica e eletrolítica e a administração intravenosa de haloperidol são a melhor abordagem terapêutica para a fase aguda da síndrome e evitar com completo a exposição ao THC, a única medida eficaz e definitiva de tratamento a longo prazo.
Domine a prescrição com segurança
A Síndrome de Hiperêmese Canabinoide reforça um princípio central da boa prática médica: não existe fármaco isento de risco — existe prescrição bem indicada, titulada e monitorada. Diferenciar uso terapêutico supervisionado de toxicidade por THC exige domínio da fisiopatologia, da farmacologia e dos critérios clínicos de segurança.
A Certificação da WeCann Academy foi estruturada para médicos que buscam prescrever cannabis com base em evidências, critérios técnicos e responsabilidade clínica.
Conheça a Certificação WeCann: Formação médica fundamentada em ciência, segurança e aplicação clínica.

Referências
- Russo EB, Spooner C, May L, Leslie R, Whiteley VL. Cannabinoid Hyperemesis Syndrome Survey and Genomic Investigation. Cannabis Cannabinoid Res. 2022;7(3):336-344.
- Montagner P, De Salas-Quiroga A. Tratado de Medicina Endocanabinoide. 1. ed. WeCann Endocannabinoid Global Academy, 2023.
- DeVuono MV, Parker LA. Cannabinoid Hyperemesis Syndrome: A Review of Potential Mechanisms. Cannabis Cannabinoid Res. 2020;5(2):132-144.
- Hopkins CY, Gilchrist BL. A case of cannabinoid hyperemesis syndrome caused by synthetic cannabinoids. J Emerg Med. 2013;45(4):544-546.
- Allen JH, de Moore GM, Heddle R, Twartz JC. Cannabinoid hyperemesis: cyclical hyperemesis in association with chronic cannabis abuse. Gut. 2004;53(11):1566-1570.
- Parker LA, Rock EM, Limebeer CL. Regulation of nausea and vomiting by cannabinoids. Br J Pharmacol. 2011;163(7):1411-1422.
- Wasilewski A, Lewandowska U, Mosinska P, et al. Cannabinoid receptor type 1 and mu-opioid receptor polymorphisms are associated with cyclic vomiting syndrome. Am J Gastroenterol. 2017;112(6):933-939.
- Richards JR, Lapoint JM, Burillo-Putze G. Cannabinoid hyperemesis syndrome: potential mechanisms for the benefit of capsaicin and hot water hydrotherapy. Clin Toxicol (Phila). 2018;56(1):15-24.
- Ruberto AJ, Sivilotti MLA, Forrester S, et al. Intravenous haloperidol versus ondansetron for cannabis hyperemesis syndrome (HaVOC). Ann Emerg Med. 2021;77(6):613-619.
