A Doença de Alzheimer (DA) é a forma mais comum de demência, representando um grande desafio para a saúde pública global. Com o envelhecimento progressivo da população mundial, estima-se que o número de pessoas afetadas pela DA triplicará até 2050, chegando a mais de 132 milhões de casos.¹ A doença está associada a graves impactos físicos, psicológicos, sociais e econômicos, não apenas para os pacientes, mas também para suas famílias e sistemas de saúde em todo o mundo. Diante desse cenário, é constante a busca por novas abordagens terapêuticas que possam prevenir, retardar ou até reverter os efeitos devastadores da DA.
Nesse contexto, os canabinoides, particularmente o canabidiol (CBD), têm atraído atenção crescente como potenciais agentes terapêuticos para a DA. O CBD é um dos principais componentes não psicotrópicos da Cannabis sativa e possui uma ampla gama de propriedades farmacológicas, incluindo efeitos anti-inflamatórios, antioxidantes e neuroprotetores. Neste post, vamos explorar o potencial do CBD no tratamento da DA, com foco em seus mecanismos de ação e evidências científicas.
Veja nessa postagem
Doença de Alzheimer
A Doença de Alzheimer é uma condição neurodegenerativa progressiva que representa a forma mais comum de demência, afetando milhões de pessoas em todo o mundo, principalmente idosos. Caracterizada pela perda gradual da memória e de outras funções cognitivas, a DA interfere de maneira significativa na capacidade do indivíduo de realizar atividades diárias.
A fisiopatologia da DA é marcada pela presença de duas principais lesões cerebrais: as placas senis, compostas por depósitos extracelulares de peptídeos beta-amiloide (Aβ), e os emaranhados neurofibrilares, formados por agregados intracelulares de proteína tau hiperfosforilada. Essas lesões se acumulam principalmente no córtex cerebral e no hipocampo, regiões críticas para a memória e o aprendizado.²
O acúmulo de beta-amiloide e tau leva a uma cascata de eventos patológicos, incluindo disfunção sináptica, neuroinflamação, estresse oxidativo e, eventualmente, morte neuronal. Esses processos resultam em uma deterioração progressiva das funções cognitivas e na manifestação de sintomas como perda de memória, confusão mental, desorientação, mudanças de humor e comportamento, e, nos estágios avançados, perda da capacidade de comunicação e da independência funcional.³
O manejo farmacológico da Doença de Alzheimer frequentemente envolve o uso de inibidores da acetilcolinesterase, como donepezila, rivastigmina e galantamina, além de memantina. Embora esses medicamentos possam melhorar temporariamente a função cognitiva e a qualidade de vida, suas limitações e efeitos colaterais são significativos. Donepezila, por exemplo, pode causar náuseas, diarreia e insônia, enquanto a rivastigmina pode levar a efeitos adversos gastrointestinais e reações cutâneas. A galantamina pode provocar efeitos colaterais semelhantes aos da donepezila, com adição de sintomas como dores de cabeça e tontura. A memantina, que age de forma diferente ao modular o sistema glutamatérgico, pode causar efeitos colaterais como tontura, cefaleia e constipação.4
Além dos medicamentos específicos para a Doença de Alzheimer, fármacos como antipsicóticos, ansiolíticos, benzodiazepínicos e antidepressivos são frequentemente empregados para manejar sintomas comportamentais e psicológicos associados à essa patologia. No entanto, cada classe possui limitações significativas. Antipsicóticos, como risperidona e olanzapina, podem aumentar o risco de sedação excessiva, ganho de peso e efeitos extrapiramidais. Já os ansiolíticos e benzodiazepínicos, como diazepam e lorazepam, frequentemente causam sedação, confusão e um risco elevado de quedas, especialmente preocupante em idosos.5
Antidepressivos, como sertralina e fluoxetina, também apresentam potenciais efeitos colaterais, incluindo disfunção gastrointestinal e alterações no apetite. Esses efeitos adversos, quando somados, podem impactar de forma negativa a qualidade de vida dos pacientes. Assim, o manejo desses medicamentos deve ser realizado com cautela e atenção, considerando a vulnerabilidade do paciente idoso e buscando minimizar riscos no contexto do tratamento da Doença de Alzheimer.
Atualmente, as opções de tratamento para a DA são limitadas e focam principalmente em aliviar os sintomas, sem modificar significativamente o curso da doença. No entanto, avanços na pesquisa sobre a fisiopatologia da DA estão direcionando novos esforços terapêuticos, com ênfase em intervenções que possam retardar ou prevenir a progressão da doença, como o uso de canabinoides, incluindo o canabidiol, que está sendo investigado por seus potenciais efeitos neuroprotetores e anti-inflamatórios.
O Sistema Endocanabinoide na Doença de Alzheimer
O sistema endocanabinoide (SEC) desempenha um papel crucial na regulação de diversas funções fisiológicas no cérebro, como a modulação da neurotransmissão, neuroproteção, e controle da neuroinflamação, que são diretamente relevantes para a Doença de Alzheimer. Este sistema é composto principalmente por receptores canabinoides (CB1 e CB2), endocanabinoides como a anandamida (AEA) e o 2-araquidonoilglicerol (2-AG), e enzimas responsáveis pela síntese e degradação desses compostos.
Estudos revelam que o SEC é afetado pela DA, com alterações significativas na expressão e funcionalidade dos receptores canabinoides, especialmente CB1 e CB2, ao longo do curso da doença. Nos estágios iniciais da DA, observa-se um aumento na expressão do receptor CB1 em áreas como o hipocampo, provavelmente como um mecanismo compensatório para mitigar o estresse neurodegenerativo.4 No entanto, à medida que a doença progride, observa-se uma redução na expressão desses receptores, associada a um declínio cognitivo mais acentuado.7 Essa dinâmica pode refletir a incapacidade do sistema endocanabinoide de manter sua função neuroprotetora em fases avançadas da doença.
Por outro lado, a expressão dos receptores CB2 é significativamente aumentada, principalmente em resposta à ativação microglial e à neuroinflamação sustentada, característica da DA.5 A ativação desses receptores tem demonstrado efeitos neuroprotetores em modelos animais, como a redução da deposição de placas amiloides (Aβ) e a diminuição da resposta inflamatória microglial, que são marcadores importantes da progressão da DA.8
Além dos receptores CB1 e CB2, outros componentes do SEC, como os receptores TRPV1 (receptor vaniloide do tipo 1) e os receptores PPARγ (receptores ativados por proliferadores de peroxissoma gama), também estão envolvidos na modulação da neuroinflamação e da neurodegeneração na DA. A ativação desses receptores por fitocanabinoides como o canabidiol e o Δ9-tetraidrocanabinol (THC) tem demonstrado potencial em mitigar os processos patológicos associados à DA, incluindo o estresse oxidativo e a disfunção mitocondrial.9
Além dos canabinoides, os terpenos também têm mostrado potencial terapêutico em estudos pré-clínicos. O β-cariofileno, um terpeno que atua nos receptores CB2 e PPARγ, demonstrou melhorar o fenótipo em modelos animais de DA, enquanto o linalol foi capaz de reverter as marcas histopatológicas da DA e restaurar funções cognitivas e emocionais, principalmente através de seus efeitos anti-inflamatórios.10 e 11
Como podemos ver, a figura abaixo ilustra de forma esquemática as principais descobertas pré-clínicas relacionadas aos mecanismos moleculares que sustentam os potenciais efeitos neuroprotetores dos fitocanabinoides THC e CBD na Doença de Alzheimer. Esses mecanismos incluem a modulação de processos neuroinflamatórios, a redução do estresse oxidativo, e a inibição da formação de placas beta-amiloide e emaranhados neurofibrilares. Ao atuar sobre receptores específicos, como CB1, CB2, TRPV1 e PPARγ, esses compostos têm demonstrado capacidade de mitigar os danos neuronais e retardar a progressão da neurodegeneração associada à DA, oferecendo uma promissora abordagem terapêutica baseada em evidências.
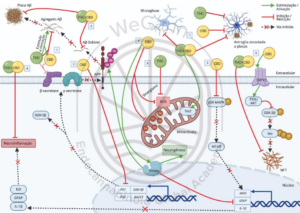
Para aprofundar seus conhecimento no sistema endocanabinoide acesse: O que é o Sistema Endocanabinoide? (wecann.academy)
Evidências Científicas
Nos últimos anos, um número crescente de estudos metodologicamente qualificados têm explorado o potencial terapêutico do canabidiol na Doença de Alzheimer. Mais de 100 pesquisas já investigaram diretamente os efeitos do sistema endocanabinoide e dos derivados canabinoides no contexto da DA, com ênfase em mecanismos moleculares e possíveis abordagens terapêuticas.
Em 2015, van den Elsen e colaboradores conduziram um ensaio clínico randomizado (ECR) que investigou o impacto de uma dose baixa de THC (1,5 mg, três vezes ao dia) por três semanas em pacientes com demência. Embora os resultados não tenham mostrado uma melhora significativa nos sintomas neuropsiquiátricos, o tratamento foi bem tolerado e apresentou um perfil de segurança favorável, com eventos adversos mínimos.12
Além disso, dois estudos-piloto subsequentes aumentaram a dosagem para 15 mg de THC por dia, e em outro para uma combinação de 9 mg de THC e 18 mg de CBD diariamente. Coletivamente, esses estudos relataram que o tratamento com canabinoides não apenas foi bem tolerado, mas também resultou em melhorias significativas nas alterações comportamentais, além de atenuar a rigidez de membros e facilitar os cuidados diários em pacientes com demência grave.13
Em 2022, Hermush et al. realizaram um ECR em Israel para investigar a segurança e a eficácia de um óleo de cannabis rico em CBD (30% de CBD e 1% de THC) em pacientes com demência. O estudo concluiu que o tratamento reduziu significativamente a agitação psicomotora em comparação com o placebo, com a maioria dos efeitos colaterais sendo leves e de curta duração.14
As propriedades ansiolíticas, antioxidantes e anti-inflamatórias do CBD, já bem documentadas em outras condições, também têm sido investigadas como potenciais benefícios para pacientes com DA. Estudos indicam que o CBD pode reduzir a ansiedade, melhorar a qualidade do sono, e atenuar sintomas como agitação e agressividade, que são comumente observados em pacientes com DA.
Além disso, evidências sugerem que o CBD pode desempenhar um papel neuroprotetor, ajudando a mitigar a produção de proteínas beta-amiloide e tau, que são fatores críticos no desenvolvimento e progressão da DA. Essas descobertas posicionam o CBD e outros derivados canabinoides como uma terapêutica promissora na abordagem da DA, oferecendo uma nova perspectiva no manejo de sintomas comportamentais e possivelmente ajudando a retardar, também, a progressão da doença.
Conclusão
O canabidiol emerge como uma abordagem terapêutica promissora para a Doença de Alzheimer, destacando-se por suas propriedades neuroprotetoras, anti-inflamatórias e antioxidantes. Embora as evidências científicas atuais sejam encorajadoras, com melhorias observadas em sintomas comportamentais e potencial neuroproteção, é necessário aprofundar a pesquisa clínica para determinar a eficácia e segurança a longo prazo do CBD em pacientes com DA.
Diante do crescente impacto global da doença e das limitações dos tratamentos convencionais, o CBD oferece uma nova perspectiva, contribuindo para o avanço de estratégias mais eficazes no combate a essa desafiadora condição neurodegenerativa. Nesse contexto, iniciativas como a WeCann desempenham um papel fundamental ao fornecer informações científicas atualizadas e recursos técnicos qualificados para profissionais da área médica.
Aprofunde seus conhecimentos a respeito da cannabis medicina: Tratado de Medicina Endocanabinoide | WeCann Academy – Wecann
Referências
- Irwin, K.,Sexton, C., Daniel, T., Lawlor, B. & Naci,L Healthy Aging and Dementia: Two Roads Diverging in Midlife? Front. Aging Neurosci. 10, 275 (2018).
- Kumar, A., Singh, A., & Ekavali. A review on Alzheimer’s disease pathophysiology and its management: an update. Pharmacol. Rep. 67, 195- 203 (2015).
- Abubakar, M, B, et al, Alzheimer’s Disease: An Update and Insights Into Pathophysiology. Front Aging Neurosci. 14, 742408 (2022).
- Forlenza, O. V.. (2005). Tratamento farmacológico da doença de Alzheimer. Archives of Clinical Psychiatry (são Paulo), 32(3), 137–148. https://doi.org/10.1590/S0101-60832005000300006.
- Auchewski, L., Andreatini, R., Galduróz, J. C. F., & Lacerda, R. B. de .. (2004). Avaliação da orientação médica sobre os efeitos colaterais de benzodiazepínicos. Brazilian Journal of Psychiatry, 26(1), 24–31. https://doi.org/10.1590/S1516-44462004000100008
- Manuel, I, de San Román, E. G, Giralt, M. T., Ferrer, I. & Rodriguez-Puertas, R. Type-1 Cannabinoid Receptor Activity During Alzheimer’s Disease Progression.J. Alkheimers Dis. 42,761-766 (2014).
- López, A. et al. Cannabinoid CB2 receptors in the mouse brain: relevance for Alzheimer’s disease. J. Neuroinflammation 15, 158 (2018).
- Coles, M., Stciner-Lim, G.Z.& Karl, T.Therapeutic properties of multi-cannabinoid treatment strategies for Alzheimer’s disease. Front. Neurosci. 16,962922 (2022).
- Berry, A.J Zubko, O., Reeves, S. J. & Howard, R.J. Endocannabinoid system alterations in Alzheimer’s disease: A systematic review of human studies. Brain Res. 1749, 147 135 (2020).
- Cheng, Y. Dong, Z. & Liu, S. B-Caryophyllene Ameliorates the. Alzheimer-Like Phenotype in APP/ P51 Mice through CB2 Receptor Activation and the PPAR-y Pathway. Pbarmacology 94, 1-12 (2014).
- Sabogal-Guáqueta, A. M., Osorio, E, & Cardona- Gómez, G. P. Linalool reverses neuropathological and behavioral impairments in old triple transgenic Alzhcimer’s mice. Neuropbarmacology 102, 111- 120 (2016).
- Van Den Elsen, G. A. H. et al.’Tetrahydrocannabinol for neuropsychiatric symptoms in dementia: A randomized controlled trial. Neurology 84, 2338- 2346 (2015).
- Broers, B. et al. Prescription ofa THC/CBD-Based Medication to Patients with Dementia: A Pilot Study in Geneva.Med.Cannabis Cannabinoids 2, 56-59 (2019).
- Hermush, V. et al. Effects of rich cannabidiol oil on behavioral disturbances in patients with dementia: A placebo controlled randomized clinical trial. Front, Med. 9, 951889 (2022).
- MONTAGNER,Patrícia; DE SALAS-QUIROGA, Adán. Tratado de Medicina Endocanabinoide.1. ed. WeCann Endocannabinoid Global Academy, 2023.
