A quimioterapia permanece como um dos pilares fundamentais no tratamento do câncer, sendo responsável por salvar incontáveis vidas. No entanto, apesar de sua eficácia contra células cancerígenas, este tratamento é frequentemente acompanhado por efeitos colaterais severos que comprometem significativamente a qualidade de vida dos pacientes.
Nos últimos anos, pesquisadores e profissionais de saúde têm investigado alternativas para mitigar esses efeitos adversos. Entre as opções que surgiram, os canabinoides têm demonstrado um potencial considerável. É crucial destacar que o THC já possui um histórico comprovado e robusto nesse campo. Medicamentos como o dronabinol e a nabilona, ambos análogos sintéticos do THC, são exemplos de fármacos registrados e amplamente utilizados para tratar efeitos secundários da quimioterapia, como náuseas e vômitos intensos, com resultados significativos.
Além do THC, o canabidiol (CBD), outro composto proeminente e não-psicotrópico da Cannabis sativa, também tem emergido como uma opção terapêutica promissora. Neste post vamos explorar como o CBD pode contribuir para a redução dos efeitos colaterais da quimioterapia, especialmente náuseas, vômitos e dor, melhorando assim a qualidade de vida dos pacientes oncológicos.
Veja nessa postagem
Efeitos colaterais da quimioterapia e seu impacto na Qualidade de Vida
A quimioterapia representa um dos pilares fundamentais no tratamento do câncer, tendo revolucionado o campo da oncologia desde sua introdução na década de 1940. Este método terapêutico consiste na administração de medicamentos citotóxicos que atuam de forma sistêmica no organismo, visando destruir células cancerígenas ou retardar seu crescimento e proliferação. Diferentemente de abordagens localizadas como a cirurgia ou radioterapia, a quimioterapia tem a capacidade de atingir células malignas em qualquer parte do corpo, tornando-se particularmente valiosa no tratamento de cânceres metastáticos ou disseminados.
Os agentes quimioterápicos são classificados em diversas categorias, incluindo agentes alquilantes, antimetabólitos, antibióticos antitumorais, inibidores de topoisomerase e alcaloides vegetais, entre outros. Cada classe atua por mecanismos distintos, mas compartilham o objetivo comum de interferir no ciclo celular e nos processos de divisão e replicação das células cancerígenas. Esta abordagem pode ser empregada com diferentes finalidades: como tratamento curativo, visando a eliminação completa da doença; como terapia neoadjuvante, para reduzir o tamanho tumoral antes de cirurgia; como tratamento adjuvante, para eliminar células cancerígenas residuais após procedimentos cirúrgicos; ou como tratamento paliativo, para controlar sintomas e melhorar a qualidade de vida em pacientes com doença avançada.
Os efeitos colaterais da quimioterapia manifestam-se em um espectro amplo e variado, afetando múltiplos sistemas e funções orgânicas. A natureza e gravidade destes efeitos dependem de diversos fatores, incluindo o tipo e dosagem dos medicamentos administrados, a duração do tratamento, características individuais do paciente como idade, estado nutricional e condições de saúde preexistentes, bem como a presença de tratamentos concomitantes como radioterapia.
As náuseas e vômitos induzidos pela quimioterapia (NVIQ) figuram entre os efeitos colaterais mais temidos e debilitantes do tratamento oncológico. Estima-se que entre 70-80% dos pacientes submetidos à quimioterapia experimentem algum grau de NVIQ, com intensidade variável conforme o potencial emetogênico do regime quimioterápico empregado. Agentes como cisplatina, dacarbazina e ciclofosfamida em altas doses são particularmente associados a episódios graves de náuseas e vômitos.
Estes sintomas podem se manifestar em diferentes padrões temporais: as náuseas e vômitos agudos ocorrem dentro das primeiras 24 horas após a administração do quimioterápico, frequentemente atingindo seu pico nas primeiras 5-6 horas; as náuseas e vômitos tardios desenvolvem-se após 24 horas e podem persistir por até 5-7 dias. As náuseas e vômitos antecipatórios, um fenômeno condicionado que surge antes mesmo da administração da quimioterapia, ocorrendo em até 25% dos pacientes e representando um desafio terapêutico particular por sua natureza psicológica.
A fisiopatologia das NVIQ envolve a ativação de vias neuroquímicas complexas, incluindo a liberação de neurotransmissores como serotonina, substância P e dopamina, que estimulam a zona de gatilho quimiorreceptora no tronco cerebral e o centro do vômito. Além disso, há envolvimento de vias aferentes vagais e esplâncnicas que transmitem sinais do trato gastrointestinal para o sistema nervoso central. Quando persistentes, as NVIQ podem levar a complicações severas como desidratação, desequilíbrios eletrolíticos, desnutrição com perda de peso significativa e deterioração do estado geral, potencialmente resultando em hospitalizações e interrupções ou modificações do esquema terapêutico planejado.
A dor associada à quimioterapia constitui outro aspecto significativo da toxicidade do tratamento. A neuropatia periférica induzida por quimioterapia (NPIQ) afeta aproximadamente 30-40% dos pacientes oncológicos. Esta condição caracteriza-se por dor neuropática, frequentemente descrita como queimação, formigamento ou sensação de choque elétrico, acompanhada de parestesias, disestesias e déficits sensoriais que tipicamente iniciam-se nas extremidades distais e progridem.
A NPIQ resulta da lesão direta às fibras nervosas periféricas pelos agentes quimioterápicos, envolvendo mecanismos como disfunção mitocondrial, estresse oxidativo, alterações na homeostase do cálcio intracelular e neuroinflamação. Em muitos casos, estes sintomas persistem mesmo após a conclusão do tratamento, tornando-se uma sequela crônica que compromete significativamente a funcionalidade e qualidade de vida a longo prazo.
Para saber mais sobre o papel do Canabidiol no tratamento da dor neuropática acesse: Canabidiol no tratamento da Dor Neuropática – WeCann Academy
Outros efeitos colaterais significativos incluem mielossupressão, resultando em neutropenia (com risco aumentado de infecções potencialmente fatais), anemia (causando fadiga extrema e dispneia) e trombocitopenia (com risco hemorrágico), alopecia, que apesar de não representar risco físico, tem profundo impacto psicológico, toxicidade gastrointestinal manifestando-se como diarreia, constipação e anorexia, disfunção cognitiva, cardiotoxicidade, hepatotoxicidade, nefrotoxicidade e toxicidade pulmonar, entre outros.
O impacto dos efeitos colaterais da quimioterapia na qualidade de vida dos pacientes oncológicos transcende as manifestações físicas, permeando dimensões psicológicas, sociais e existenciais da experiência humana.
Na dimensão física, a fadiga extrema (presente em 70-100% dos pacientes) compromete significativamente a autonomia para atividades cotidianas. A dor crônica, especialmente na forma de neuropatia periférica, limita a mobilidade e destreza. Alterações na imagem corporal como alopecia e mudanças de peso afetam a autoestima e podem levar a disfunções sexuais persistentes.
Psicologicamente, os pacientes enfrentam taxas elevadas de depressão (15-25%) e ansiedade, particularmente antes das sessões de tratamento e exames. O medo da recorrência da doença, preocupações com dependência e incertezas quanto ao futuro constituem fontes adicionais de sofrimento mental.
No âmbito social, o tratamento frequentemente resulta em isolamento devido às hospitalizações recorrentes e ao tempo dedicado ao gerenciamento dos efeitos colaterais. O estigma associado ao câncer pode exacerbar esse isolamento. Muitos pacientes enfrentam dificuldades profissionais, precisando reduzir jornadas de trabalho ou abandonar suas carreiras, com consequente impacto financeiro e perda de identidade profissional.
Náuseas e vômitos persistentes contribuem significativamente para anorexia, perda de peso e condicionamento psicológico negativo. A dor neuropática, geralmente refratária a analgésicos convencionais, compromete o bem-estar físico e emocional mesmo após a conclusão do tratamento.
Em suma, os efeitos colaterais da quimioterapia representam um fardo significativo para pacientes oncológicos, impactando negativamente múltiplas dimensões da qualidade de vida. A compreensão abrangente deste impacto é fundamental para o desenvolvimento de estratégias eficazes de manejo dos sintomas e suporte integral aos pacientes, visando não apenas a maximização da sobrevida, mas também a preservação da qualidade de vida durante e após o tratamento do câncer.
Mecanismos de Ação do CBD: Interação com o Sistema Endocanabinoide
O canabidiol (CBD) possui mecanismos de ação complexos e multifacetados que podem explicar sua eficácia potencial no controle de náuseas e vômitos induzidos pela quimioterapia. Diferentemente do tetrahidrocanabinol (THC), o CBD não atua primariamente como agonista direto dos receptores canabinoides CB1 e CB2, mas interage com o sistema endocanabinoide de maneiras distintas.²
Tem sido proposto que o CBD atue como um modulador alostérico negativo do receptor CB1, o que significa que pode alterar a configuração deste receptor, reduzindo a capacidade de ligação de agonistas como o THC. Este mecanismo pode explicar por que o CBD parece capaz de atenuar alguns dos efeitos psicoativos do THC quando administrados conjuntamente.²
O canabidiol inibe a enzima amida hidrolase de ácidos graxos (FAAH), responsável pela degradação da anandamida, um endocanabinoide endógeno. Estudos em animais demonstraramque a inibição resulta em níveis aumentados de anandamida, prolongando seus efeitos no sistema nervoso central e periférico, o que pode contribuir para os efeitos anti-náusea e antiemético.²
Além disso, o CBD também interage com o sistema serotoninérgico, particularmente com os receptores 5-HT1A e 5-HT3A. Esta interação representa um ponto de convergência importante entre o sistema endocanabinoide e o sistema serotoninérgico na regulação de náuseas e vômitos.
O CBD parece atuar como um modulador alostérico nos receptores 5-HT3A, reduzindo a eficácia do 5-HT (serotonina) de maneira dependente da concentração. Esta ação é semelhante à dos antagonistas clássicos do receptor 5-HT3, como o ondansetrona (OND), que são amplamente utilizados como antieméticos na prática clínica oncológica.³
Paralelamente, o CBD potencializa indiretamente a ação da serotonina endógena nos autorreceptores 5-HT1A. A ativação destes receptores resulta em feedback negativo, diminuindo a liberação adicional de serotonina. Este mecanismo é particularmente relevante porque a elevação de serotonina no córtex insular interoceptivo (CII) está implicada na gênese da náusea, e o CBD pode prevenir esta elevação.³
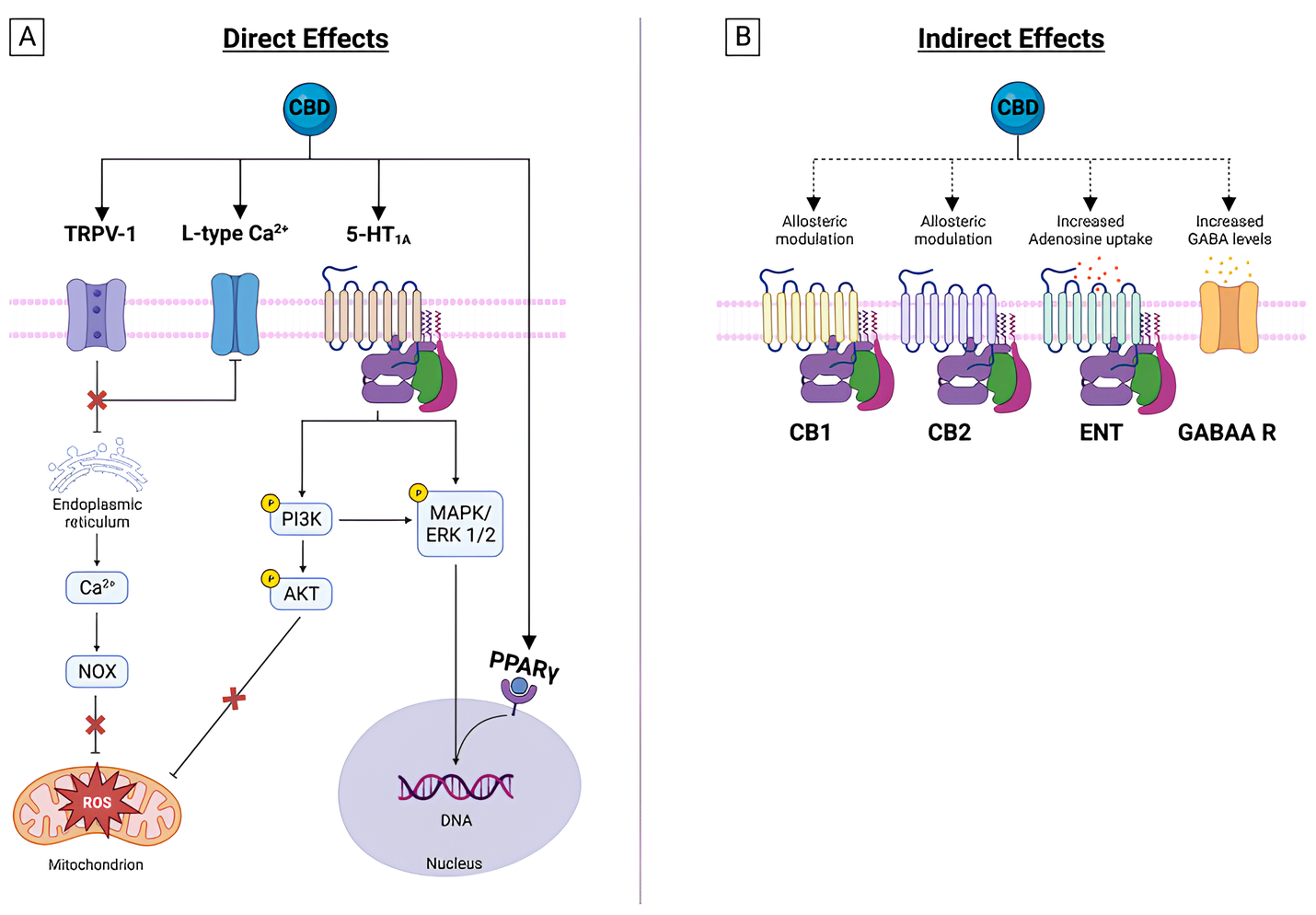
Além disso, o sistema endocanabinoide está intimamente envolvido na modulação da dor. O CBD atua de forma mais ampla, ele ativa e, subsequentemente, dessensibiliza os receptores vaniloides (TRPV1). Esses receptores, que são considerados parte de uma “visão estendida” do sistema endocanabinoide, estão diretamente envolvidos na transmissão da dor e da inflamação. A dessensibilização do TRPV1 é um mecanismo chave que pode levar à analgesia (alívio da dor).4
O CBD também demonstra propriedades anti-inflamatórias através da inibição de citocinas pró-inflamatórias e modulação da atividade de células imunes. Estas ações podem atenuar a mucosite oral e gastrointestinal causada pela quimioterapia, condições inflamatórias dolorosas que comprometem significativamente a qualidade de vida e nutrição dos pacientes.²
O “chemobrain” (disfunção cognitiva relacionada à quimioterapia) é um efeito colateral debilitante. As propriedades neuroprotetoras do CBD, mediadas pela modulação do estresse oxidativo e neuroinflamação, podem potencialmente atenuar o declínio cognitivo induzido pela quimioterapia. O sistema endocanabinoide desempenha papel crucial na plasticidade neural e função cognitiva, fornecendo base teórica para esta aplicação.
Para saber mais sobre os efeitos da cannabis na excitabilidade cerebral acesse: Efeitos da Cannabis na Excitabilidade Cerebral – WeCann Academy
O sistema endocanabinoide desempenha um papel fundamental na manutenção da homeostase corporal, incluindo a regulação das funções gastrointestinais. Ao modular esse sistema, o CBD pode ajudar a restaurar o equilíbrio alterado pelos agentes quimioterápicos, destacando-se como um candidato promissor no manejo dos efeitos colaterais da quimioterapia.
Evidências científicas
O potencial analgésico do CBD, especialmente em combinação com THC em proporções controladas, tem se mostrado significativo no contexto oncológico. A revisão sistemática de Darkovska-Serafimovska et al. (2018) evidenciou efeito analgésico em 15 dos 18 ensaios clínicos analisados, com doses médias eficazes de 25 mg de CBD/dia combinadas com 27 mg de THC/dia. Este padrão de dosagem equilibrada entre CBD e THC parece oferecer melhor controle da dor com minimização dos efeitos psicotrópicos.5
Em estudo com 232 pacientes oncológicos com dor, Pawasarat et al. (2020) demonstraram que o grupo tratado com cannabis medicinal contendo CBD (137 pacientes) apresentou melhora significativa nos escores de avaliação de sintomas ESAS (Edmonton Symptom Assessment System), além de redução expressiva no consumo de opioides – até 33%. Esta redução no uso de medicamentos opioides representa um benefício particularmente relevante, considerando os riscos de dependência e efeitos adversos associados à terapia opioide de longo prazo.6
As evidências científicas mais consistentes apontam para a eficácia do CBD especificamente no tratamento da dor neuropática, incluindo aquela induzida por agentes quimioterápicos. Este tipo de dor, frequentemente resistente aos analgésicos convencionais, representa um desafio significativo no manejo de pacientes oncológicos. Em reconhecimento a estas evidências, tanto a Federação Europeia de Dor quanto a Sociedade Canadense de Dor posicionaram as formulações canabinoides contendo CBD como medicamentos de terceira linha no manejo da dor neuropática.7
A pesquisa sobre o potencial dos canabinoides no alívio dos efeitos colaterais da quimioterapia tem avançado, com diversos estudos clínicos explorando formulações que combinam CBD e THC.
Grimison et al. (2020) conduziram um ensaio clínico randomizado multicêntrico duplo-cego de fase II/III avaliando uma formulação oral equilibrada de CBD:THC (2,5 mg de cada, três vezes ao dia) para prevenção de náuseas e vômitos induzidos por quimioterapia. Os resultados foram promissores, com aumento nas taxas de resposta completa de 14% para 25%. Embora 31% dos pacientes tenham experimentado efeitos adversos como sedação e vertigem, a aceitabilidade da terapia foi notável, com 83% dos participantes preferindo a formulação contendo CBD ao placebo para controle sintomático.8
Duran et al. (2010) relataram resultados ainda mais expressivos utilizando nabiximols, um spray oromucoso contendo proporções equilibradas de CBD (2,5 mg/mL) e THC (2,7 mg/mL). Este estudo demonstrou um impressionante aumento nas respostas completas de 22% para 71% nos pacientes que utilizaram a formulação (n = 17), com doses médias diárias de 12 mg de CBD e 13 mg de THC. A alta aceitabilidade dos pacientes quanto aos efeitos colaterais desta formulação contendo CBD sugere um perfil de segurança favorável.9
Pesquisa mais recente conduzida por Sukpiriyagul et al. (2023) corrobora estes achados. Em um ensaio clínico randomizado duplo-cego cruzado realizado na Tailândia, os pesquisadores avaliaram uma preparação oral de CBD:THC (1:1) em 54 pacientes com câncer ginecológico submetidos à quimioterapia com potencial emetogênico moderado a alto. A conclusão foi que o tratamento à base de cannabis contendo CBD representa um agente adjuvante apropriado para reduzir náuseas e vômitos induzidos pela quimioterapia.10
Um impressionante estudo israelita acompanhou quase 3.000 pacientes com câncer tratados com cannabis medicinal entre 2015 e 2017. Após seis meses de uso, dos 1.211 pacientes que completaram o estudo, 95,9% relataram melhora em sua condição, enquanto apenas 0,3% relataram piora. Os benefícios específicos foram abrangentes: 74% dos pacientes reduziram sintomas de ansiedade e depressão, 70% reduziram distúrbios do sono, 55% reduziram a fadiga, e 54% reduziram sintomas de náuseas e vômitos.11
É fundamental ressaltar que, nos estudos apresentados, as formulações utilizadas continham tanto CBD quanto THC. Portanto, não é possível atribuir os benefícios observados exclusivamente ao CBD, uma vez que o THC, conhecido por suas propriedades antieméticas e analgésicas, também estava presente e pode ter contribuído significativamente para os resultados. A interação entre esses canabinoides, conhecida como “efeito entourage”, é uma área de pesquisa contínua.
As evidências científicas indicam que o CBD é um aliado promissor no manejo dos efeitos colaterais da quimioterapia, contribuindo para o controle da dor neuropática, náuseas, distúrbios do sono e fadiga. Além de reduzir a dependência de opioides, seu uso melhora o bem-estar emocional e a adesão ao tratamento oncológico. A continuidade da pesquisa nesta área almeja refinar a compreensão e otimizar o uso clínico do CBD, melhorando a qualidade de vida de pacientes oncológicos em tratamento quimioterápico.
Conclusão
O impacto dos efeitos colaterais da quimioterapia na qualidade de vida dos pacientes oncológicos é significativo, afetando tanto o bem-estar físico quanto o psicológico. Nesse contexto, o CBD apresenta um potencial terapêutico relevante, modulando o sistema endocanabinoide e interagindo com vias neuroquímicas envolvidas no controle de náuseas, vômitos e dor neuropática. Seu perfil de segurança e ações anti-inflamatórias fazem dele uma alternativa interessante no manejo dos sintomas adversos do tratamento oncológico.
A individualização do tratamento e a supervisão médica são essenciais para garantir eficácia e segurança. À medida que novas pesquisas avançam, o CBD pode se tornar uma ferramenta cada vez mais relevante no suporte a pacientes em tratamento quimioterápico, contribuindo para uma melhor qualidade de vida e adesão ao tratamento. Neesse sentido, para que a incorporação do canabidiol na prática clínica ocorra de forma segura e eficaz, é essencial que os médicos tenham acesso a informações atualizadas e baseadas em evidências científicas.
Nesse contexto, a Comunidade da WeCann Academy se destaca como um espaço fundamental para essa atualização, oferecendo uma rede global de profissionais altamente capacitados. Nesse ambiente colaborativo, os médicos e acadêmicos trocam conhecimentos, discutem casos clínicos desafiadores e exploram novas estratégias terapêuticas, garantindo que estejam sempre preparados para implementar as abordagens mais eficazes no tratamento com cannabis medicinal.
Além disso, a WeCann se destaca pela sua estrutura educativa, oferecendo ferramentas práticas e recursos de fácil acesso. As “WeCann Talks” e os “WeCann Rounds” proporcionam discussões dinâmicas sobre os mais recentes protocolos de tratamento, permitindo que os médicos compartilhem insights e tirem dúvidas diretamente com especialistas de renome. O aplicativo da WeCann garante que a educação e o networking possam ser acessados a qualquer hora e de qualquer lugar, promovendo uma verdadeira revolução no ensino médico. Ao fazer parte dessa comunidade, os médicos não só aprimoram suas habilidades terapêuticas, mas também garantem que seus pacientes recebam cuidados mais personalizados e eficazes.
Referências
- Silveira FM, Wysocki AD, Mendez RDR, Pena SB, Santos EM dos, Malaguti-Toffano S, et al.. Impacto do tratamento quimioterápico na qualidade de vida de pacientes oncológicos. Acta paul enferm [Internet]. 2021;34:eAPE00583. Available from: https://doi.org/10.37689/acta-ape/2021AO00583
- MONTAGNER, Patrícia; DE SALAS-QUIROGA, Adán. Tratado de Medicina Endocanabinoide.1. ed. WeCann Endocannabinoid Global Academy, 2023.
- Rock, Erin M et al. “Therapeutic Potential of Cannabidiol, Cannabidiolic Acid, and Cannabidiolic Acid Methyl Ester as Treatments for Nausea and Vomiting.” Cannabis and cannabinoid research vol. 6,4 (2021): 266-274. doi:10.1089/can.2021.0041
- Iannotti FA, Hill CL, Leo A, Alhusaini A, Soubrane C, Mazzarella E, Russo E, Whalley BJ, Di Marzo V, Stephens GJ. Nonpsychotropic plant cannabinoids, cannabidivarin (CBDV) and cannabidiol (CBD), activate and desensitize transient receptor potential vanilloid 1 (TRPV1) channels in vitro: potential for the treatment of neuronal hyperexcitability. ACS Chem Neurosci. 2014 Nov 19;5(11):1131-41. doi: 10.1021/cn5000524. Epub 2014 Jul 29. PMID: 25029033.
- Darkovska-Serafimovska M, Serafimovska T, Arsova-Sarafinovska Z, Stefanoski S, Keskovski Z, Balkanov T. Pharmacotherapeutic considerations for use of cannabinoids to relieve pain in patients with malignant diseases. J Pain Res. 2018 Apr 23;11:837-842. doi: 10.2147/JPR.S160556. PMID: 29719417; PMCID: PMC5922297.
- Pawasarat IM, Schultz EM, Frisby JC, Mehta S, Angelo MA, Hardy SS, Kim TWB. The Efficacy of Medical Marijuana in the Treatment of Cancer-Related Pain. J Palliat Med. 2020 Jun;23(6):809-816. doi: 10.1089/jpm.2019.0374. Epub 2020 Feb 26. PMID: 32101075.
- Liang, A. L., Gingher, E. L & Coleman, ]. S. Medical Cannabis for Gynecologic Pain Conditions: A Systematic Review. Obstet. Gymecol. 139,287-296 (2022).
- Grimison P, Mersiades A, Kirby A, Lintzeris N, Morton R, Haber P, Olver I, Walsh A, McGregor I, Cheung Y, Tognela A, Hahn C, Briscoe K, Aghmesheh M, Fox P, Abdi E, Clarke S, Della-Fiorentina S, Shannon J, Gedye C, Begbie S, Simes J, Stockler M. Oral THC:CBD cannabis extract for refractory chemotherapy-induced nausea and vomiting: a randomised, placebo-controlled, phase II crossover trial. Ann Oncol. 2020 Nov;31(11):1553-1560. doi: 10.1016/j.annonc.2020.07.020. Epub 2020 Aug 13. PMID: 32801017.
- Duran M, Pérez E, Abanades S, Vidal X, Saura C, Majem M, Arriola E, Rabanal M, Pastor A, Farré M, Rams N, Laporte JR, Capellà D. Preliminary efficacy and safety of an oromucosal standardized cannabis extract in chemotherapy-induced nausea and vomiting. Br J Clin Pharmacol. 2010 Nov;70(5):656-63. doi: 10.1111/j.1365-2125.2010.03743.x. PMID: 21039759; PMCID: PMC2997305.
- Sukpiriyagul A, Chartchaiyarerk R, Tabtipwon P, Smanchat B, Prommas S, Bhamarapravatana K, Suwannarurk K. Oral Tetrahydrocannabinol (THC):Cannabinoid (CBD) Cannabis Extract Adjuvant for Reducing Chemotherapy-Induced Nausea and Vomiting (CINV): A Randomized, Double-Blinded, Placebo-Controlled, Crossover Trial. Int J Womens Health. 2023 Aug 16;15:1345-1352. doi: 10.2147/IJWH.S401938. PMID: 37608911; PMCID: PMC10440684.
- Bar-Lev Schleider,L. et al. Prospective analysis of safety and efficacy of medical cannabis in large unselected population of patients with cancer. Enr. J. Intern. Med. 49, 37-43 (2018).
- Martinez Naya, Nadia et al. “Molecular and Cellular Mechanisms of Action of Cannabidiol.” Molecules (Basel, Switzerland) vol. 28,16 5980. 9 Aug. 2023, doi:10.3390/molecules28165980
