O transtorno por uso de álcool (TUA) é uma condição psiquiátrica caracterizada pelo consumo descontrolado de álcool, e todas as suas consequências negativas. Atinge milhões de pessoas em todo o mundo e representa um grande desafio para a saúde pública, devido às suas complicações médicas, sociais e psicológicas. Tratamentos tradicionais, como terapia farmacológica e comportamental, apresentam taxas variadas de sucesso, destacando a necessidade de novas abordagens terapêuticas.
Nos últimos anos, o canabidiol (CBD), um dos principais compostos não psicotrópico da planta Cannabis sativa, tem emergido como uma opção promissora no manejo do TUA, devido às suas propriedades neuroprotetoras, ansiolíticas e moduladoras do sistema endocanabinoide. No post de hoje iremos explorar o papel do canabidiol no manejo terapêutico do transtorno por uso de álcool.
Veja nessa postagem
Transtorno por uso de álcool
O Transtorno por Uso de Álcool é uma condição psiquiátrica multifacetada, caracterizada pelo consumo compulsivo de álcool. Esse consumo gera diversas consequências negativas para a saúde física, mental e social. O álcool é a substância psicoativa legal mais consumida no Brasil e, embora amplamente aceito socialmente, seu uso abusivo constitui um grave problema de saúde pública. Farmacologicamente, o álcool é classificado como uma droga depressora do sistema nervoso central, promovendo inicialmente euforia e desinibição, seguidos por disfunções cognitivas e motoras à medida que inibe a atividade neuronal.¹
Atualmente, a Organização Mundial da Saúde (OMS) define a dependência de álcool como uma síndrome caracterizada pelo uso contínuo da substância, mesmo diante de danos significativos à saúde física e mental, bem como prejuízos nas relações interpessoais e no funcionamento social e econômico. O impacto do consumo abusivo de álcool é globalmente devastador, sendo responsável por aproximadamente 2,5 milhões de mortes anualmente, o que o posiciona como a terceira principal causa de morte evitável no mundo. No Brasil, as taxas de mortalidade relacionadas ao consumo de álcool são particularmente altas, afetando 8,2% dos homens e 3,2% das mulheres.
Do ponto de vista clínico, o diagnóstico de TUA abrange um conjunto de critérios definidos pelo Diagnostic and Statistical Manual of Mental Disorders (DSM-5), que incluem sintomas comportamentais e fisiológicos, como a presença de fissura, abstinência e comprometimentos em diversas áreas funcionais. Os sintomas de abstinência podem variar desde alterações no sono e apetite até manifestações autonômicas como bradicardia e tremores, refletindo o impacto sistêmico do álcool sobre o organismo.
Tradicionalmente, o tratamento do TUA envolve uma combinação de intervenções farmacológicas e psicoterapêuticas. Entre as abordagens psicoterápicas, a Terapia Cognitivo-Comportamental (TCC) tem se mostrado eficaz em muitos casos, ajudando os pacientes a identificar e modificar padrões de pensamento disfuncionais, que perpetuam o ciclo de consumo de álcool. No entanto, a TCC clássica apresenta limitações, especialmente em pacientes com comorbidades psiquiátricas, como transtornos de personalidade, que tendem a apresentar altas taxas de recaída.¹
Além das terapias psicossociais, o manejo farmacológico do TUA inclui o uso de medicamentos como o dissulfiram, naltrexona e acamprosato, que atuam em diferentes vias neuroquímicas para reduzir o desejo pelo álcool e os sintomas de abstinência. No entanto, a resposta ao tratamento varia amplamente entre os pacientes, refletindo a complexidade da dependência alcoólica e a necessidade de abordagens terapêuticas personalizadas.¹
Diante das limitações dos tratamentos convencionais, novas abordagens estão sendo investigadas, incluindo o uso de canabinoides no manejo do TUA. O canabidiol, tem demonstrado potencial neuroprotetor e ansiolítico, além de modular o sistema endocanabinoide, que está envolvido na regulação de processos emocionais e de recompensa associados à dependência de substâncias. Estudos científicos sugerem que o CBD pode ser uma intervenção promissora para reduzir o consumo de álcool e aliviar os sintomas de abstinência.
TUA e Sistema Endocanabinoide
O CBD exerce efeitos terapêuticos por meio de vários mecanismos de ação. Um dos principais é sua interação com o sistema endocanabinoide (SEC), que desempenha um papel fundamental na regulação de funções como humor, estresse, prazer e dependência. O SEC é composto por receptores canabinoides, como o CB1 e o CB2, e seus ligantes endógenos, os endocanabinoides. No TUA, o consumo excessivo de álcool altera o funcionamento deste sistema, contribuindo para a dependência e recaída.³
O sistema endocanabinoide desempenha um papel crucial na regulação dos circuitos neuronais associados ao sistema de recompensa, um mecanismo central no desenvolvimento de Transtornos por Uso de Substâncias (TUS), incluindo o Transtorno por Uso de Álcool. Este sistema neuronal é fundamental para o reforço positivo de comportamentos relacionados ao prazer e ao consumo de substâncias, sendo composto por neurotransmissores como dopamina, glutamato e ácido gama-aminobutírico (GABA). A influência do SEC sobre o sistema de recompensa pode ter implicações significativas para a compreensão e o manejo do TUA.³
Os receptores canabinoides CB1 são elementos fundamentais na modulação do sistema de recompensa, particularmente na área tegmental ventral (VTA). A ativação dos receptores CB1 nesta região reduz a liberação de GABA, resultando na desinibição dos neurônios dopaminérgicos e subsequente ativação do sistema mesocorticolímbico. Este processo é fundamental para o reforço de comportamentos de busca por substâncias e para a manutenção do consumo compulsivo de álcool.4
O receptor CB2, embora menos estudado em comparação ao CB1, também desempenha um papel significativo no TUA. A manipulação farmacológica do CB2 tem demonstrado afetar comportamentos relacionados à dependência de álcool. Modelos animais com deleção genética do CB2 exibem aumento no consumo de álcool e maior propensão à recaída.5 Além disso, análises de tecido cerebral post-mortem de indivíduos com alcoolismo revelaram alterações na expressão do gene CNR2, que codifica o receptor CB2. Essas alterações genéticas e suas correlações com o TUA indicam que o receptor CB2 pode ser um alvo potencial para intervenções terapêuticas.
Um dos principais mecanismos pelo qual o CBD atua é como um modulador alostérico negativo dos receptores CB1. Isso significa que o CBD pode alterar a forma como os receptores CB1 respondem a seus ligantes naturais ou a outras substâncias, resultando em efeitos neuromodulatórios, que podem atenuar a busca compulsiva por álcool. O CBD, ao agir como um modulador alostérico negativo dos receptores CB1, pode alterar a resposta dos neurônios dopaminérgicos à ativação do sistema de recompensa. Isso pode resultar em uma diminuição na compulsão por álcool e na redução dos comportamentos associados à dependência.³
Embora o CBD não se ligue diretamente aos receptores CB2, ele pode influenciar a expressão e a atividade destes receptores de forma indireta. A modulação do CB2 pelo CBD pode contribuir para a redução dos comportamentos de busca por álcool e ajudar a prevenir recaídas. Além da interação com o SEC, o CBD atua por meio de outros mecanismos neurobiológicos que podem contribuir para o tratamento do TUA. O CBD possui propriedades ansiolíticas e antipsicóticas, que são atribuídas em parte à sua interação com os receptores serotoninérgicos 5-HT1a e aos receptores dopaminérgicos D2. Essas ações podem ajudar a reduzir a ansiedade e a compulsão associadas ao consumo de álcool.6,7
Para saber mais sobre o Sistema Endocanabinoide acesse: O que é o Sistema Endocanabinoide?
Evidências científicas
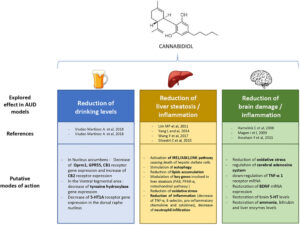
As evidências científicas têm demonstrado que o CBD possui propriedades neuroprotetoras significativas. Em modelos animais de TUA, o CBD tem mostrado reduzir os danos cerebrais induzidos pelo álcool, especificamente nas regiões do hipocampo e do córtex entorrinal, áreas críticas para a memória e a cognição.8 Estes efeitos são particularmente importantes, pois a neurodegeneração nessas regiões está associada a déficits cognitivos e comportamento impulsivo, fatores que podem contribuir para a recaída no TUA.9
Além dos efeitos neuroprotetores, o CBD também tem mostrado potencial na prevenção da hepatotoxicidade induzida pelo álcool. Estudos pré-clínicos revelaram que o CBD pode prevenir aumentos nas enzimas hepáticas ALT e AST, que são marcadores de danos ao fígado.10 Essa proteção hepática é particularmente relevante para pacientes com TUA, que frequentemente apresentam problemas hepáticos devido ao consumo excessivo de álcool.
Um estudo, conduzido com camundongos C57BL/6J machos, uma raça conhecida por sua preferência por etanol, demonstrou que a administração de CBD reduziu as propriedades de reforço, a motivação e a recaída associadas ao etanol. Em doses crescentes (30, 60 e 120 mg/kg), administradas por via intraperitoneal, o CBD diminuiu a preferência por etanol (de 75% para 55%) e a ingestão (de cerca de 6 g/kg/dia para 3,5 g/kg/dia) em um paradigma de escolha entre água e solução de etanol a 8%. Esses resultados foram corroborados por um paradigma operante, onde camundongos pressionavam uma alavanca para obter acesso a 36 mL de solução de etanol a 8%.11
O CBD também reduziu o número de prensas de alavanca ativas em aproximadamente 40% e a motivação para beber etanol em cerca de 50%, além de diminuir a recaída em cerca de 30% após uma sessão de extinção com uma dose de 120 mg/kg. O tratamento com CBD não afetou a motivação para a ingestão de água. Além disso, o CBD foi eficaz na redução da hipotermia e convulsões induzidas por etanol, mas não influenciou a concentração de etanol no sangue.11
Conclusão
Diante das evidências apresentadas, o canabidiol emerge como uma alternativa promissora no tratamento do Transtorno por Uso de Álcool, oferecendo tanto neuroproteção quanto modulação dos sistemas envolvidos no comportamento compulsivo e na dependência. Seus efeitos sobre o sistema endocanabinoide, aliados às suas propriedades ansiolíticas e hepatoprotetoras, o colocam como uma abordagem terapêutica inovadora.
No entanto, é fundamental que mais estudos clínicos em humanos sejam realizados para validar esses achados pré-clínicos e estabelecer protocolos seguros e eficazes para o uso do CBD no manejo do TUA, possibilitando assim, uma nova fronteira no tratamento da dependência alcoólica. Nesse contexto, a WeCann desempenha um papel essencial ao fornecer conteúdos técnicos de qualidade, sempre baseados em rigor científico, contribuindo para a incorporação segura da cannabis medicinal na prática médica e promovendo uma abordagem mais assertiva e personalizada no manejo de pacientes portadores de TUA.
Referências
- Maciel, Luisa & Tractenberg, Saulo & Habigzang, Luísa & Wainer, Ricardo. (2013). Esquemas iniciais desadaptativos no transtorno por uso de álcool. Revista Brasileira de Terapias Cognitivas. 9. 101-107. 10.5935/1808-5687.20130014.
- American Psychiatric Association (APA) (2014). DSM-5: Manual diagnóstico e estatístico de transtornos mentais: DSM-5. (5 ed.) Porto Alegre: Artmed.
- MONTAGNER,Patrícia; DE SALAS-QUIROGA, Adán. Tratado de Medicina Endocanabinoide.1. ed. WeCann Endocannabinoid Global Academy, 2023.
- Sagheddu, C., Muntoni, A. L, Pistis, M. & Melis, M. Endocannabinoid Signaling in Motivation, Reward, and Addiction. in International Review of Neurobiology vol. 125 257-302 (Elsevier, 2015).
- García-Gutiérrez, M.S. et al. Role of Cannabinoid CB2 Receptor in Alcohol Use Disorders: From Animal to Human Studies. Int.J. Mol. Sci. 23, 5908 (2022).
- Paulus, V., Billieux, J, Benyamina, A. & Karila, L. Cannabidiol in the context of substance use disorder treatment: A systematic review. Addict. Bebav. 132, 107360 (2022).
- Navarrete, F, García-Gutiérrez, M. S., Gasparyan, A., Austrich-Olivares, A. & Manzanares, J. Role of Cannabidiol in the Therapeutic Intervention for Substance Use Disorders. Front. Pharmacol. 12, 626010 (2021).
- Hamelink C, Hampson A, Wink DA, Eiden LE, Eskay RL. Comparison of cannabidiol, antioxidants, and diuretics in reversing binge ethanol-induced neurotoxicity. J Pharmacol Exp Ther. 2005 Aug;314(2):780-8. doi: 10.1124/jpet.105.085779. Epub 2005 May 5. PMID: 15878999; PMCID: PMC4183207.
- Stevens L, Goudriaan AE, Verdejo-Garcia A, Dom G, Roeyers H, Vanderplasschen W. Impulsive choice predicts short-term relapse in substance-dependent individuals attending an in-patient detoxification programme. Psychol Med. 2015 Jul;45(10):2083-93. doi: 10.1017/S003329171500001X. Epub 2015 Feb 2. PMID: 25640022.
- Wang Y, Mukhopadhyay P, Cao Z, Wang H, Feng D, Haskó G, Mechoulam R, Gao B, Pacher P. Cannabidiol attenuates alcohol-induced liver steatosis, metabolic dysregulation, inflammation and neutrophil-mediated injury. Sci Rep. 2017 Sep 21;7(1):12064. doi: 10.1038/s41598-017-10924-8. PMID: 28935932; PMCID: PMC5608708.
- Viudez-Martínez A, García-Gutiérrez MS, Navarrón CM, Morales-Calero MI, Navarrete F, Torres-Suárez AI, Manzanares J. Cannabidiol reduces ethanol consumption, motivation and relapse in mice. Addict Biol. 2018 Jan;23(1):154-164. doi: 10.1111/adb.12495. Epub 2017 Feb 13. PMID: 28194850.
- De Ternay, J., Naassila, M., Nourredine, M., Louvet, A., Bailly, F., Sescousse, G., Maurage, P., Cottencin, O., Carrieri, P. M., & Rolland, B. (2019). Therapeutic prospects of cannabidiol for alcohol use disorder and alcohol-related damages on the liver and the brain. Frontiers in Pharmacology, 10. Disponível em: https://www.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2019.00627. DOI: 10.3389/fphar.2019.00627.
