O dogma de que o cérebro não se regenera após um evento agudo foi superado. Este artigo explora as bases moleculares da neuroplasticidade e demonstra como o Sistema Endocanabinoide (SEC) atua como um regulador mestre na contenção de danos secundários pós-AVC, Traumatismo Cranioencefálico (TCE) e lesões medulares. Aprofunde-se nos mecanismos de neuroproteção mediados por fitocanabinoides (como o CBD) — desde o bloqueio da excitotoxicidade glutamatérgica e transição microglial (M1 para M2), até a promoção da neurogênese hipocampal e regeneração axonal.
Veja nessa postagem
O Mito do Neurônio Irrecuperável
Durante décadas, a neurociência manteve uma crença quase dogmática: neurônios mortos não voltam. Se uma região do cérebro fosse danificada — por um Acidente Vascular Cerebral (AVC), um Traumatismo Cranioencefálico (TCE), uma Encefalopatia Hipóxico-Isquêmica (EHI) ou uma Lesão Medular (LME) — sua função estaria perdida para sempre. Essa visão, embora compreensível dado o estado do conhecimento da época, hoje sabemos que está incompleta.
A descoberta da neurogênese no cérebro adulto mudou radicalmente esse paradigma. Experimentos pioneiros, como o realizado em 1965 com autorradiografia em cérebros de ratos — onde a incorporação de H³-timidina apontou o giro denteado do hipocampo como sítio ativo de formação de novos neurônios — demonstraram que o processo de criação neuronal contínua ao longo de toda a vida adulta.¹
A neuroplasticidade e a regeneração celular representam, portanto, a fronteira do reparo do sistema nervoso após eventos agudos. Compreender como o Sistema Endocanabinoide (SEC) atua nesses cenários é fundamental, pois ele opera como um regulador central da homeostase e do destino celular.²
O que são Canabinoides?
Os canabinoides são compostos químicos biologicamente ativos que interagem com o SEC, uma complexa rede de sinalização presente em todos os vertebrados. Eles são classificados em três categorias principais:²
• Endocanabinoides: Moléculas produzidas naturalmente pelo organismo, como a anandamida (AEA) e o 2-araquidonoilglicerol (2-AG).
• Fitocanabinoides: Compostos de origem vegetal encontrados na Cannabis sativa, sendo o THC (∆⁹-tetraidrocanabinol) e o CBD (canabidiol) os mais estudados.
• Canabinoides Sintéticos: Criados em laboratório para mimetizar ou modular a atividade dos receptores canabinoides, muito usados em pesquisa científica.
O que é Neuroplasticidade e Regeneração?
A neuroplasticidade é a capacidade contínua do cérebro de se reorganizar, formar novas conexões sinápticas e adaptar-se a novas situações ou danos. A regeneração refere-se ao processo de reparo e recuperação tecidual após uma lesão aguda, envolvendo a proliferação de células-tronco, o crescimento de novos axônios e a restauração da barreira hematoencefálica e da mielina.²
No cérebro adulto, dois nichos principais foram identificados como zonas ativas de neurogênese: a Zona Subventricular (SVZ) do ventrículo lateral e a Zona Subgranular (SGZ) do hipocampo. O processo de maturação de um novo neurônio pode levar de 2 a 4 meses, desde a proliferação até a plena integração no circuito neural.¹
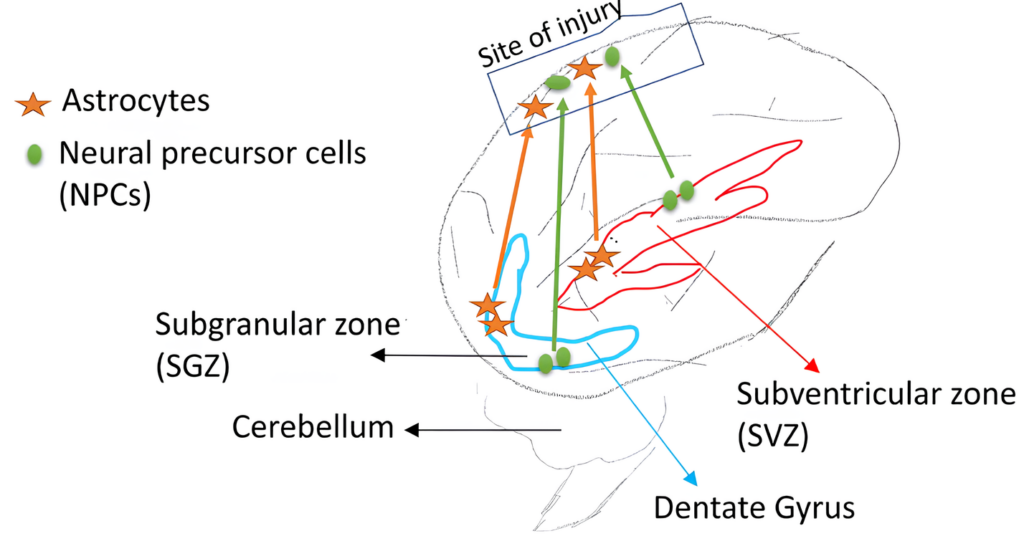
Nichos celulares da zona subventricular (SVZ) e da zona subgranular (SGZ) no sistema nervoso central dos mamíferos adultos. Astrócitos e células precursoras neurais (NPCs) são ricos em SGZ e SVZ. Sob efeito de lesão cerebral, NPCs e astrócitos dentro de nichos neurogênicos são ativados e podem migrar para o local da lesão. Fonte: Sallam, Abeer & Mousa, Shaker. (2020). Neurodegenerative Diseases and Cell Reprogramming. Molecular Neurobiology. 57. 10.1007/s12035-020-02039-5.
O Sistema Endocanabinoide no Trauma
Após um insulto cerebral grave — como trauma ou privação de oxigênio —, o cérebro sofre inflamação severa e excesso de toxinas naturais. O SEC é imediatamente ativado para tentar conter esse dano. O pesquisador Vincenzo Di Marzo resumiu as funções do SEC como: “comer, dormir, relaxar, esquecer e proteger”. Os fitocanabinoides auxiliam esse sistema agindo como neuroprotetores: reduzem a inflamação, bloqueiam a morte de células nervosas e estimulam o crescimento de novos neurônios.²
Resposta Bifásica à Lesão do SNC
Após um evento agudo (AVC, TCE ou LME), o SNC apresenta duas fases distintas:
Na fase aguda, ocorre resposta inflamatória agressiva, excitotoxicidade e morte celular. Nesse momento, há liberação compensatória massiva dos endocanabinoides AEA e 2-AG, que ativam receptores CB1 para controlar o estresse oxidativo e o dano vascular.
Na fase crônica ou prolongada, a AEA diminui, mas os níveis de 2-AG aumentam notavelmente, atuando de forma preferencial nos receptores CB2, que ficam superexpressos nessa fase.
Mecanismos de Neuroproteção e Reparo
O “Freio” contra a Excitotoxicidade
Em traumas ou hipóxia, ocorre liberação excessiva e descontrolada de glutamato, o principal neurotransmissor excitatório, causando a morte dos neurônios por hiperestimulação — a chamada excitotoxicidade. O SEC age por meio de sinalização retrógrada: o 2-AG é produzido sob demanda no neurônio pós-sináptico e viaja de volta à fenda sináptica para ativar o CB1 no neurônio pré-sináptico. Essa ativação bloqueia os canais de cálcio, interrompendo abruptamente a liberação de glutamato — funcionando como um verdadeiro “disjuntor de segurança” para a sobrevivência neuronal.³
Modulação da Neuroinflamação e Células da Glia
A neuroinflamação é orquestrada pela micróglia e pelos astrócitos. No dano agudo, essas células assumem um fenótipo M1 (pró-inflamatório), liberando citocinas que ampliam a lesão tecidual, e passam a expressar altos níveis de receptores CB2. A utilização de canabinoides agonistas do CB2 induz a micróglia a transicionar para o fenótipo M2 (anti-inflamatório e reparador), criando um microambiente que permite a depuração de detritos celulares e a regeneração tecidual subsequente.²
Estudos de knockout demonstraram que camundongos sem CB1 apresentam redução significativa na proliferação celular no giro denteado e diminuição no número total de novos neurônios — confirmando seu papel indispensável na neurogenese hipocampal. Curiosamente, a ausência de CB2 não altera a neurogenese basal, sugerindo que esse receptor atua principalmente sob condições de demanda aumentada, como nos processos inflamatórios e neurodegenerativos.¹
Mielinização e Preservação da Barreira Hematoencefálica (BHE)
A falha da BHE é um dos principais agravantes da injúria secundária. Estudos mostram que a intervenção com canabinoides reduz a hipóxia tecidual e diminui a liberação do Fator de Crescimento Endotelial Vascular (VEGF), protegendo as junções da BHE. Adicionalmente, fitocanabinoides favorecem a sobrevivência de oligodendrócitos, fundamental para a remielinização de tratos axonais sobreviventes após isquemia ou trauma.6
Essa remielinização foi confirmada em modelos experimentais com WIN-55212-2, que promoveu a diferenciação de oligodendrócitos progenitores por meio da regulação da fosforilação de ERK1/2 via CB1, e também com CBD em modelos de isquemia, onde houve aumento do marcador MAP-2 e regeneração dendrítica.¹
Vias moleculares: Os Receptores CB1, CB2 e o crescimento Axonal
O CB1 predomina no hipocampo, córtex cerebral, gânglios da base e cerebelo, e é o principal alvo do THC e da AEA. Sua ativação dispara cascatas de sinalização que incluem as vias PI3K/AKT, ERK e BDNF — todas relacionadas à sobrevivência neuronal, proliferação de progenitores e diferenciação celular.¹
O receptor GPR55, expresso em células-tronco neurais (NSCs) humanas e murinas, quando ativado pelo agonista O-1602 aumenta a proliferação de NSCs e o número de neurônios imaturos no hipocampo. O receptor nuclear PPARγ também integra o sistema, sendo um dos mecanismos pelos quais o CBD exerce efeitos neuroprotetores e pró-neurogênicos, especialmente em modelos de Alzheimer e doença de Huntington.¹
Os receptores CB1 e CB2 estão intrinsecamente ligados ao controle da morfogênese, especificação de linhagens neurais e navegação axonal. A ativação dos receptores canabinoides na membrana plasmática de células progenitoras neurais desencadeia vias de sinalização intracelular de sobrevida primordiais, incluindo a fosfatidilinositol 3-quinase (PI3K/Akt), a cascata ERK/MAPK e a modulação da via mTOR.¹
Na Lesão da Medula Espinhal (LME), a inibição da enzima MAGL — que aumenta os níveis endógenos de 2-AG — ou a estimulação direta do CB1 demonstraram ativar a via PI3K/pAkt, promovendo uma robusta regeneração axonal no gânglio da raiz dorsal. Esse mecanismo foi validado por Martinez-Torres et al. (2023), que estabeleceram que a sinalização endocanabinoide promove a regeneração de axônios após lesão nervosa, mediada pelas vias CB1 e PI3K/Akt.4
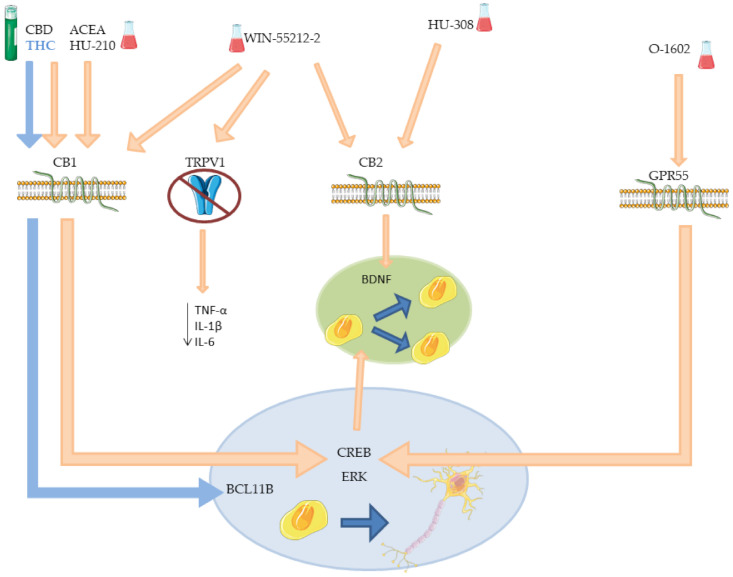
Mecanismo dos diferentes fitocanabinoides sintéticos na neurogênese. A imagem oferece uma representação esquemática dos receptores envolvidos na neurogênese e sua cascata de sinais ativada após a ação agonista de fitocanabinoides sintéticos, testados em células ou animais que não se assemelham a nenhuma doença específica. O efeito do THC no BCL11B é destacado em azul. BCL11B: Linfoma/leucemia de células B 11B; BDNF: fator neurotrófico derivado do cérebro; CREB: proteína de ligação a elementos de resposta cAMP; ERK: quinases reguladas por sinal extracelular. Fonte: Valeri A, Mazzon E. Cannabinoids and Neurogenesis: The Promised Solution for Neurodegeneration? Molecules. 2021;26(20):6313. https://doi.org/10.3390/molecules26206313
A Curva Dose-Resposta do CBD: Por que a titulação dita o sucesso neurogênico.
O potencial neuroprotetor do CBD é multidirecional e não depende exclusivamente dos receptores CB1/CB2. O CBD ativa o receptor de adenosina A2a, modula os receptores 5-HT1A e ativa receptores nucleares PPARγ, regulando a proliferação e diferenciação de células-tronco no hipocampo.²
No contexto do TCE, a neurogênese mediada pelo CBD segue uma resposta complexa: doses baixas tendem a estimular a neurogênese, enquanto doses muito elevadas em indivíduos não estressados podem inibi-la — provavelmente pela dessensibilização dos receptores. Curiosamente, em cenários de estresse crônico ou dano neural severo, o efeito pró-neurogênico das altas doses de CBD é mantido, destacando a necessidade de titulação baseada no contexto fisiopatológico.¹
Essa dualidade foi documentada por Aychman et al. (2023), que identificaram os múltiplos alvos moleculares do CBD frente ao trauma craniano, com modulação na neurogênese hipocampal e proteção independente dos receptores glutamatérgicos.5
Essa dualidade não é um fenômeno isolado do contexto traumático; ela representa uma característica farmacodinâmica dos fitocanabinoides. A chamada curva bifásica — ou efeito em “U invertido” — demonstra que doses baixas podem estimular neurogênese e modular positivamente a plasticidade sináptica, enquanto doses excessivamente elevadas podem atenuar ou até inibir esses mesmos processos. Em neuroproteção, portanto, mais não significa melhor.
Evidências por Contexto Clínico: AVC, TCE, Hipóxia Neonatal e Lesão Medular.
Acidente Vascular Cerebral (AVC)
O CBD (10 mg/kg) melhorou o desempenho cognitivo de camundongos após isquemia cerebral, aumentou o número de neurônios DCX-positivos, elevou os níveis de BDNF no hipocampo e promoveu regeneração dendrítica. O WIN-55212-2 protegeu oligodendrócitos na penumbra isquêmica, promoveu remielinização e aumentou neuroblastos em modelos de hipóxia-isquemia neonatal. O JWH-133 (agonista seletivo de CB2) estimulou a migração de neuroblastos para o corpo caloso após AVC.¹
Hemorragia Intraventricular
Del Pozo et al. (2024) comprovaram que a administração de CBD diminuiu o dano cerebral, reduziu a dilatação ventricular em 81% e preservou a mielina em modelos de hemorragia intraventricular em murinos prematuros — evidenciando proteção estrutural e funcional significativa em um cenário de altíssima morbimortalidade.6
Encefalopatia Hipóxico-Isquêmica (EHI)
Pazos et al. (2012) evidenciaram que o CBD modula a excitotoxicidade a curto prazo e restaura o desempenho neurocomportamental e a integridade cognitiva duradoura em modelos de EHI neonatal, indicando forte reparo funcional mediado pelo SEC.³
Traumatismo Cranioencefálico (TCE)
Aychman et al. (2023) documentaram os múltiplos alvos moleculares do CBD frente ao trauma craniano, com modulação na neurogênese hipocampal, redução de neuroinflamação e proteção independente dos receptores glutamatérgicos.5
Lesão Medular (LME)
A sinalização endocanabinoide via CB1 e PI3K/Akt promoveu regeneração axonal no gânglio da raiz dorsal em modelos de LME — efeito confirmado tanto pela inibição de MAGL (aumento de 2-AG endógeno) quanto pela estimulação direta do receptor.²
Doença de Alzheimer (DA)
O CBD (10 mg/kg) reduziu a neuroinflamação causada por depósitos de Aβ, diminuiu a ativação microglial, reduziu GFAP (gliose) e promoveu neurogenese no giro denteado — efeitos mediados por PPARγ. O CBD também aumentou sinaptofisina e sinapsina I (marcadores de formação sináptica) e ativou o receptor TrkA, alvo do NGF.¹
Embora esses achados derivem majoritariamente de modelos experimentais, eles dialogam diretamente com os pilares fisiopatológicos da doença: neuroinflamação crônica, disfunção sináptica e perda progressiva de conectividade. A redução de GFAP, a modulação microglial e o estímulo à neurogênese no giro denteado sugerem que o impacto do CBD pode transcender o controle comportamental, alcançando dimensões estruturais da degeneração.
Doença de Parkinson (DP)
O AM-1241 (agonista de CB2) regenerou neurônios dopaminérgicos em modelo de DP induzido por MPTP, restaurando a expressão de CB2, Parkin/PINK1 e PI3K/AKT na substância negra. CBD e cannabigerol (CBG) regularam positivamente receptores dopaminérgicos D2 e D4 em células NSC-34, com implicações para plasticidade sináptica.¹
Estresse Crônico e Ansiedade
O CBD (30 mg/kg) reverteu a supressão de neurogênese hipocampal induzida por estresse crônico, aumentou NeuN+ (neurônios maduros) e produziu efeito ansiolítico dependente da neurogênese — quando esta era bloqueada farmacologicamente, o efeito ansiolítico desaparecia. A ação foi CB1-dependente e associada a aumento de AEA por inibição de FAAH.¹
A nova fronteira terapêutica na reabilitação neurológica.
A neuroplasticidade — essa capacidade dinâmica do cérebro de reorganizar circuitos, formar novas conexões e, em determinados contextos, gerar novos neurônios — deixou de ser um conceito teórico para se tornar um dos pilares da neurociência contemporânea.
Nesse cenário, o Sistema Endocanabinoide (SEC) desponta como um dos reguladores mais versáteis desse processo, integrando sinalização inflamatória, homeostase sináptica, metabolismo energético e sobrevivência celular.
O canabidiol (CBD), em especial, surge como um dos compostos mais promissores dentro dessa perspectiva. Sua atuação multimodal — envolvendo receptores CB1, CB2, PPARγ, A2A e 5-HT1A — associa-se a efeitos anti-inflamatórios, preservação da barreira hematoencefálica e estímulo à sobrevivência e diferenciação neuronal em diferentes modelos experimentais. Essa convergência de mecanismos não sugere apenas controle sintomático, mas potencial modulação estrutural em cenários de lesão e neurodegeneração.
As evidências científicas são consistentes: regeneração axonal em modelos de lesão medular, proteção da mielina na hemorragia neonatal, reparo funcional na encefalopatia hipóxico-isquêmica e modulação multialvo no traumatismo cranioencefálico. Em conjunto, esses dados apontam para um papel estruturante do SEC nos processos de reparo do sistema nervoso central.
É fundamental reconhecer, contudo, que a maior parte dessas pesquisas ainda é pré-clínica. Estudos em humanos permanecem limitados, a padronização de dose e formulação representa desafio metodológico relevante, e os efeitos a longo prazo precisam ser melhor caracterizados em ensaios clínicos robustos. Ainda assim, quando diferentes modelos experimentais convergem para mecanismos semelhantes de neuroproteção e plasticidade, o sinal científico torna-se difícil de ignorar.
A pergunta que abre esta discussão — o cérebro pode se regenerar? — já não encontra a mesma resposta cética de décadas atrás. Hoje, ela é acompanhada por uma hipótese cada vez mais plausível: sim, o cérebro possui capacidade regenerativa modulável, e os canabinoides podem ocupar um papel central nessa nova etapa da medicina moderna.
Formação Clínica para Prescrição Baseada em Evidências
O avanço da neurociência nos impõe uma responsabilidade proporcional ao conhecimento disponível. Se hoje compreendemos melhor os mecanismos de neuroplasticidade, neuroinflamação e modulação sináptica, torna-se dever do médico aprofundar-se para aplicar essas evidências com rigor e segurança.
A Medicina Endocanabinoide não deve ser conduzida por tendências ou simplificações terapêuticas, mas por domínio fisiopatológico, compreensão farmacodinâmica e capacidade de individualizar condutas — especialmente em cenários neurológicos complexos.
A Certificação Internacional em Medicina Endocanabinoide da WeCann Academy foi estruturada para oferecer essa base técnica. O programa aprofunda os fundamentos da neurobiologia celular, as vias moleculares de neuroproteção, os princípios de titulação segura e a integração clínica dos fitocanabinoides em contextos como trauma, doenças neurodegenerativas e reabilitação neurológica.
A decisão de aprofundar-se não é apenas acadêmica. É um compromisso com a qualidade da prática médica e com a oferta da melhor estratégia terapêutica possível ao paciente.
[Conheça a Certificação em Medicina Endocanabinoide]
Referências
- Valeri A, Mazzon E. Cannabinoids and Neurogenesis: The Promised Solution for Neurodegeneration? Molecules. 2021;26(20):6313. https://doi.org/10.3390/molecules26206313
- Montagner P, De Salas-Quiroga A. Tratado de Medicina Endocanabinoide. 1. ed. WeCann Endocannabinoid Global Academy; 2023.
- Pazos MR, Cinquina V, Gómez A, Layunta R, Santos M, Fernández-Ruiz J, et al. Cannabidiol administration after hypoxia-ischemia to newborn rats reduces long-term brain injury and restores neurobehavioral function. Neuropharmacology. 2012;63(5):776-83.
- Martinez-Torres S, et al. Injury-induced activation of the endocannabinoid system promotes axon regeneration. iScience. 2023;26(6):106814.
- Aychman MM, Goldman DL, Kaplan JS. Cannabidiol’s neuroprotective properties and potential treatment of traumatic brain injuries. Front Neurol. 2023;14:1087011.
- Del Pozo A, de Hoz-Rivera M, Romero A, Villa M, Martínez M, Silva L, et al. Cannabidiol reduces intraventricular hemorrhage brain damage, preserving myelination and preventing blood brain barrier dysfunction in immature rats. Neurotherapeutics. 2024;21(2):e00326.
- Sallam, Abeer & Mousa, Shaker. (2020). Neurodegenerative Diseases and Cell Reprogramming. Molecular Neurobiology. 57. 10.1007/s12035-020-02039-5.
