A dor crônica é uma condição complexa e debilitante que afeta uma parcela significativa da população global, muitas vezes resultando em uma redução substancial na qualidade de vida dos pacientes. Tradicionalmente, o manejo dessa condição tem se apoiado em terapias convencionais, como o uso de AINES e derivados opioides. No entanto, o uso prolongado desses medicamentos está associado a uma série de desafios clínicos, incluindo o risco de dependência, desenvolvimento de tolerância e uma gama de efeitos adversos significativos.
Esses desafios têm motivado uma busca crescente por alternativas terapêuticas que ofereçam eficácia sem os mesmos riscos. Nesse cenário, a cannabis medicinal tem emergido como uma opção promissora, potencialmente capaz de preencher essa lacuna no tratamento da dor crônica. No post de hoje vamos explorar detalhadamente os mecanismos de ação da cannabis, sua interação com o sistema endocanabinoide e sua eficácia no manejo da dor crônica, fundamentada nas mais recentes e qualificadas evidências científicas.
Veja nessa postagem
Dor Crônica
A dor crônica é geralmente definida como uma dor que persiste por mais de 3 a 6 meses, ultrapassando o tempo normal de cura esperado para uma lesão ou condição aguda. Diferentemente da dor aguda, que serve como um sinal de alerta para o corpo, a dor crônica persiste além do seu papel fisiológico inicial, tornando-se uma condição patológica que pode resultar em significativa limitação funcional e comprometimento da qualidade de vida. A dor crônica pode ser classificada em diferentes categorias, como dor neuropática, nociceptiva, ou mista, dependendo dos mecanismos subjacentes.
- Dor Neuropática: Esta forma de dor crônica resulta de uma lesão ou disfunção do sistema nervoso, seja central (cérebro e medula espinhal) ou periférico (nervos fora do cérebro e medula). Exemplos comuns incluem neuropatia diabética, neuralgia pós-herpética e dor associada à esclerose múltipla. A dor neuropática é frequentemente descrita como uma sensação de queimação, formigamento ou choque elétrico e pode ser resistente aos analgésicos tradicionais.¹
- Dor Nociceptiva: Surge de danos aos tecidos corporais, como músculos, ossos ou órgãos internos, e é mediada pelos nociceptores, que são receptores sensoriais específicos para a dor. A dor nociceptiva pode ser somática (originária da pele, músculos ou articulações) ou visceral (originária dos órgãos internos). A dor somática é geralmente bem localizada e descrita como latejante ou pulsátil, enquanto a dor visceral tende a ser mais difusa e pode ser descrita como uma sensação de pressão ou cólica. Exemplos incluem dor associada a lesões musculoesqueléticas, como artrites ou fraturas ósseas, e dor visceral, como aquela causada por pancreatite ou cólica renal.¹
- Dor Mista: Como o nome sugere, a dor mista envolve componentes tanto neuropáticos quanto nociceptivos. Esse tipo de dor pode ocorrer em condições como lombalgia crônica, onde há envolvimento tanto de estruturas musculoesqueléticas quanto de nervos. A dor mista pode ser especialmente desafiadora de tratar, pois pode requerer uma abordagem multifacetada que aborda tanto os aspectos neuropáticos quanto os nociceptivos da dor.¹
Os sintomas da dor crônica variam amplamente e podem incluir dor constante ou intermitente, sensação de queimação, formigamento, rigidez muscular e sensibilidade exacerbada. A intensidade da dor pode oscilar de leve a severa, e muitas vezes é acompanhada por outros sintomas, como fadiga, distúrbios do sono, depressão e ansiedade. A dor crônica não apenas afeta a saúde física do paciente, mas também tem implicações significativas para a saúde mental e social, contribuindo para a incapacidade de realizar atividades diárias e para o isolamento social.²
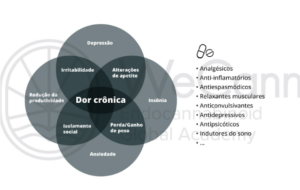
O manejo da dor crônica frequentemente envolve a prescrição de múltiplos medicamentos, um cenário conhecido como polifarmácia, que é comum devido à complexidade dessa condição. Entre os fármacos mais utilizados estão os anti-inflamatórios não esteroides (AINEs), gabapentinoides, opioides, anticonvulsivantes e antidepressivos, cada um com mecanismos de ação distintos e perfis específicos de efeitos adversos.
- AINEs: Esses medicamentos são amplamente utilizados para aliviar a dor e reduzir a inflamação. No entanto, seu uso prolongado pode causar efeitos adversos gastrointestinais graves, como úlceras e hemorragias, além de aumentar o risco de eventos cardiovasculares, como infarto do miocárdio e acidente vascular cerebral.³
- Gabapentinoides: Os gabapentinoides, incluindo gabapentina e pregabalina, são comumente prescritos para dor crônica. Esses fármacos atuam ligando-se aos canais de cálcio voltagem-dependentes nos neurônios, o que resulta na diminuição da liberação de neurotransmissores excitatórios, como o glutamato. Apesar de sua eficácia, o uso de gabapentinoides não está isento de efeitos colaterais, sendo os mais comuns a sonolência e tontura, que podem comprometer a qualidade de vida dos pacientes. Além disso, o ganho de peso é outro efeito adverso significativo, especialmente em pacientes com comorbidades, como diabetes ou doenças cardiovasculares. Em alguns casos, pode ocorrer edema periférico, causando inchaço nas extremidades, como pernas e pés.4
- IRSN: Os inibidores da recaptação de serotonina e noradrenalina, também conhecidos como antidepressivos duais, como a duloxetina e a venlafaxina, são considerados fármacos de primeira linha no tratamento da dor crônica. Em doses mais baixas, esses medicamentos agem predominantemente como os inibidores seletivos da recaptação de serotonina (ISRS), enquanto em doses mais altas, também inibem a recaptação de noradrenalina, proporcionando um efeito analgésico adicional. Essa dupla ação torna os IRSN particularmente eficazes em condições como neuropatia diabética, fibromialgia e outras síndromes de dor crônica. Contudo, assim como os ISRS, os IRSN apresentam efeitos colaterais que podem limitar seu uso. Entre os mais comuns estão náuseas, tontura, boca seca e disfunção sexual, como redução da libido ou dificuldade em atingir o orgasmo. Além disso, os IRSN podem aumentar a pressão arterial, particularmente em doses mais elevadas, o que exige monitoramento em pacientes com hipertensão ou doenças cardiovasculares.4
- Opioides: Embora sejam extremamente eficazes no controle da dor crônica severa, os opioides apresentam um risco elevado de desenvolvimento de tolerância, dependência física e psicológica. Complicações adicionais incluem constipação intestinal severa, náuseas e vômitos, e em altas doses, depressão respiratória e risco de overdose, que pode ser fatal.4
- Anticonvulsivantes e antidepressivos tricíclicos: Estes medicamentos são frequentemente utilizados no tratamento da dor neuropática. Apesar de sua eficácia, eles podem causar uma variedade de efeitos colaterais, como sonolência, tontura, ganho de peso, constipação intestinal, boca seca e, em alguns casos, impacto negativo no humor e na cognição, o que pode limitar sua utilização em alguns pacientes.6
A polifarmácia, embora frequentemente necessária para alcançar um controle adequado da dor, aumenta o risco de interações medicamentosas e pode levar a complicações adicionais, como quedas, hospitalizações e até mesmo mortalidade. Isso ocorre especialmente em pacientes com comorbidades, que já fazem uso de diversos medicamentos para condições crônicas como hipertensão, diabetes, asma ou hipotireoidismo, adicionando uma complexidade ainda maior ao regime terapêutico.
Diante das limitações e riscos associados aos tratamentos convencionais, a cannabis tem sido explorada como uma alternativa terapêutica promissora no manejo da dor crônica. Seus principais compostos ativos, tetraidrocanabinol (THC) e canabidiol (CBD), interagem com o sistema endocanabinoide, que desempenha um papel crucial na modulação da dor e da inflamação. A cannabis oferece uma abordagem multimodal ao tratamento da dor, com o potencial de reduzir a necessidade de múltiplos medicamentos, minimizando assim, o risco de interações medicamentosas e os efeitos adversos associados.
Sistema Endocanabinoide na dor crônica
O sistema endocanabinoide (SEC) desempenha um papel crucial na modulação da dor, sendo um alvo emergente para o tratamento da dor crônica. Composto por uma complexa rede de receptores, ligantes e enzimas, o SEC regula diversos processos fisiológicos, incluindo a percepção da dor e a resposta inflamatória. Este sistema envolve principalmente os endocanabinoides, como a anandamida e o 2-araquidonilglicerol (2-AG), que se ligam aos receptores canabinoides CB1 e CB2, além de outros receptores sensíveis aos endocanabinoides, como TRPV1, GPR55 e PPARs.²
Os receptores CB1 estão amplamente distribuídos no sistema nervoso central e periférico, onde modulam a transmissão nociceptiva. Quando ativados, esses receptores inibem a liberação de neurotransmissores excitatórios, como o glutamato, e reduzem a transmissão de sinais dolorosos nos neurônios sensoriais. Nos nervos periféricos, a ativação dos receptores CB1 suprime a transmissão dos estímulos nociceptivos, enquanto nos níveis espinhais e supraespinhais, esses receptores inibem a ascensão e a percepção da dor, modulando também os componentes emocionais e cognitivos associados à dor crônica.7
Os receptores CB2, por outro lado, estão predominantemente localizados em células imunológicas, como macrófagos e mastócitos, e desempenham um papel fundamental na modulação da dor inflamatória. A ativação dos receptores CB2 inibe a liberação de citocinas pró-inflamatórias, diminuindo a inflamação e, consequentemente, a sensibilidade à dor. Este mecanismo é especialmente relevante em condições onde a inflamação é um fator contribuinte significativo para a dor crônica, como na artrite reumatoide e outras doenças inflamatórias.7
Além disso, os fitocanabinoides, que interagem com os receptores canabinoides, também modulam outros sistemas de receptores, incluindo os opioides, serotoninérgicos, dopaminérgicos, colinérgicos, GABAérgicos e glutamatérgicos. Essa ampla gama de interações permite que os derivados canabinoides exerçam efeitos moduladores não apenas sobre a dor, mas também sobre o humor, apetite, sono, processos inflamatórios, memória, além de funções cardiovasculares e gastrointestinais. Essas ações combinadas contribuem para uma melhoria geral na qualidade de vida dos pacientes e reduzem a necessidade de medicamentos convencionais.
Saiba mais sobre os fitocanabinoides e suas interações com o sistema endocanabinoide: Principais Fitocanabinoides e seus efeitos no organismo (wecann.academy)
Evidências Científicas
A dor crônica é uma das principais razões que levam os pacientes a buscarem tratamento com cannabis medicinal. Esses pacientes, além de relatarem alívio da dor, frequentemente reportam melhorias no humor, apetite, padrão intestinal e padrão de sono, como observado em diversos estudos clínicos observacionais.8 Estes estudos demonstram que os derivados canabinoides podem impactar positivamente a qualidade de vida geral (QoL) e a qualidade de vida relacionada à saúde (HRQoL) dos pacientes com dor crônica, evidenciada através de questionários padronizados.9
Um estudo de coorte conduzido em Israel, envolvendo 3.000 pacientes com dor associada ao câncer, revelou que 74% dos pacientes que iniciaram o tratamento com cannabis medicinal apresentaram redução nos sintomas de ansiedade e depressão; 70% relataram melhora nos transtornos do sono; 55% relataram diminuição da fadiga; 54% tiveram uma redução nos sintomas de náusea e vômito, e mais de 36% reduziram o uso de opioides. Em média, cerca de 70% dos pacientes observaram uma melhora significativa na qualidade de vida.10
Bar-Lev Schleider et al. (2022) conduziram um estudo prospectivo relevante, também em Israel, envolvendo uma grande coorte de mais de 10.000 pacientes. Nesse estudo, 80% dos pacientes apresentavam dor crônica e transtornos do sono como os principais sintomas. Após 6 meses de tratamento com cannabis medicinal, 74,7% dos 4.166 pacientes avaliados relataram melhorias na intensidade da dor, com 64,3% relatando uma redução de 30% ou mais na dor, e 47,2% relatando uma melhora de 50% ou mais. Além disso, antes do início do tratamento, 62% dos pacientes classificaram sua dor entre 8 e 10 na escala de intensidade de dor, enquanto após 6 meses de tratamento, apenas 5% mantinham essa intensidade.11
Além da redução da dor, os pacientes também apresentaram melhoras em outros sintomas concomitantes, como redução de acessos de raiva (91,5%), inquietação (89,5%), transtornos do sono (89,1%) e náuseas (88,9%). Consequentemente, a qualidade de vida dos pacientes aumentou significativamente, com 69,9% relatando uma qualidade de vida “Boa” após 6 meses de tratamento, em comparação com apenas 12,9% antes do início do tratamento.11
A administração oromucosa de canabinoides também tem mostrado resultados promissores no controle da dor crônica. Uberall (2020) demonstrou que a coadministração de THC e CBD na proporção de 1:1, conhecida como nabiximols, é eficaz no controle da dor neuropática, com dosagens ideais variando entre 8 e 12 pulverizações diárias, correspondendo a 22-32 mg de THC e 20-30 mg de CBD.12 Resultados semelhantes foram observados em uma metanálise conduzida por Darkovska-Serafmovska et al. (2018), que confirmou a eficácia do nabiximols no manejo da dor neuropática, artrite reumatoide e dor associada ao câncer.13
Estudos com administração de cannabis via inalatória, como o ECR duplo-cego conduzido por Almog et al. (2020), demonstraram que doses tão baixas quanto 1 mg de THC, administradas através do inalador dosimetrado Syqe®, foram eficazes na produção de analgesia segura e satisfatória em pacientes com dor crônica. A via inalatória, devido ao rápido início de ação, é particularmente interessante para o manejo de episódios de dor crônica agudizada, embora a precisão da dosagem em cada inalação ainda seja um desafio.14
Conclusão
O uso de cannabis no manejo da dor crônica ressalta a relevância dessa abordagem terapêutica, especialmente em um contexto onde os tratamentos convencionais, como AINEs e opioides, apresentam limitações significativas. A evidência crescente sugere que a cannabis, com sua ação multimodal sobre o sistema endocanabinoide, pode não apenas aliviar a dor, mas também melhorar a qualidade de vida dos pacientes, reduzindo sintomas concomitantes como ansiedade, depressão e distúrbios do sono. Esses achados reforçam a necessidade de considerar a cannabis como uma opção terapêutica válida no arsenal de tratamento da dor crônica, integrando-a de forma criteriosa e baseada em evidências na prática clínica.
Portanto, é de suma importância que os médicos se mantenham atualizados sobre as melhores práticas para oferecer o melhor cuidado aos seus pacientes. Nesse contexto, a WeCann desempenha um papel fundamental ao fornecer informações atualizadas e baseadas em evidências científicas sobre a cannabis medicinal, capacitando médicos para que possam ofertar o melhor cuidado aos seus pacientes.
Referências
- Miranda CCV, Seda Junior L de F, Pelloso LRC do A. New physiological classification of pains: current concept of neuropathic pain. Rev dor [Internet]. 2016;17:2–4. Available from: https://doi.org/10.5935/1806-0013.20160037
- MONTAGNER,Patrícia; DE SALAS-QUIROGA, Adán. Tratado de Medicina Endocanabinoide.1. ed. WeCann Endocannabinoid Global Academy, 2023.
- Batlouni M. Anti-inflamatórios não esteroides: Efeitos cardiovasculares, cérebro-vasculares e renais. Arq Bras Cardiol [Internet]. 2010Apr;94(4):556–63. Available from: https://doi.org/10.1590/S0066-782X2010000400019
- Hennemann-Krause, L., & Sredni, S.. (2016). Systemic drug therapy for neuropathic pain. Revista Dor, 17, 91–94. https://doi.org/10.5935/1806-0013.20160057
- Kraychete DC, Garcia JBS, Siqueira JTT de, . Recommendations for the use of opioids in Brazil: Part IV. Adverse opioid effects. Rev dor [Internet]. 2014Jul;15(3):215–23. Available from: https://doi.org/10.5935/1806-0013.20140047
- Bortolini LGC, Kulak CAM, Boguszewski CL. Efeitos endócrinos e metabólicos dos antiepilépticos. J epilepsy clin neurophysiol [Internet]. 2008Nov;14:32–8. Available from: https://doi.org/10.1590/S1676-26492008000600006
- Maldonado, R., Baños, J. E. & Cabańero, D. The endocannabinoid system and neuropathic pain. Pain 157, S23-S32 (2016).
- Stillman, M. et al, Utilization of medicinal cannabis for pain by individuals with spinal cord injury. Spinal Cord Ser: Cases 5, 66 (2019).
- Meng, H. et al. Patient-reported outcomes in those consuming medical cannabis: a prospective longitudinal obser vational study in chronic pain patients. Can. J. Anesth, Can. Anesth, (2021) doi:10.1007/s12630-020-01903-1.
- Bar-Lev Schleider, L. et al. Prospective analysis of safety and efficacy of medical cannabis in large unselected population of patients with cancer. Eur; J. Intern. Med. 49, 37-43 (2018).
- Bar-Ley Schleider, L., Mechoulam, R., Sikorin, I., Naftali, T. & Novack, V. Adherence, Safety, and Effectiveness of Medical Cannabis and Epidemiological Characteristics of the Paticnt Population: A Prospective Study. Front. Med. 9, 827849 (2022).
- Ueberall, M., Essner, U. & Mueller-Schwefe, G. H. 38. H. Effectiveness and tolerability of THC:CBD oromucosal spray as add-on measure in patients with severe chronic pain: analysis of 12-week open- label real-world data provided by the German Pain c-Registry. J. Pain Res. Volume 12, 1577-1604 (2019). Darkovska-Serafimovska, M. et al.
- Pharmacotherapeutic considerations for use of cannabinoids o relicve pain in patients with malignant diseases.J. Pain Res. Volume 1 1, 837-842 (2018).
- Almog, S. et al. The pharmacokinetics, efficacy, and safety of a novel selective-dose cannabis inhaler in patients with chronic pain: A randomized, double- blinded, placebo-controlled trial. Eur. J. Pain 24, 1505-1516 (2020).
